Background, basic:
細胞に電極を刺してみると・・・
どうなるでしょうか?細胞は小さいのにそんな事出来るの?と思うかもしれません。ガラス管を炎で溶かしつつ引っ張り、中に濃い電解質液を入れると、極細のガラス管電極が出来上がります。科学者たちがこれを巧みに操って細胞に刺入する事に成功したのは70年くらい前の事です。高入力インピーダンスの電圧計につなぎ内外の電位差を測ると、たいていの場合、細胞内が細胞外に比べてマイナス数十mVの値を示します。静止膜電位と呼ばれるものです。乾電池が1.5 Vですので、ずいぶんと小さいと思うかもしれません。しかし、細胞膜の厚さは僅か数ナノメートルです。電場の強さとして考えてみれば、 数十[mV] / 数 [nm]=~100000 [V/cm] にも達します。
どうして・・・
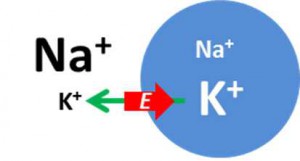
そんな事になっているのでしょうか?私たちは日々食事をとり、ミトコンドリアでエネルギー産生を行っています(ATP合成)。このエネルギーの一部は、細胞内外のイオン環境を非対称にする為に使われています。細胞膜にあるNAKAという酵素などの働きによるものです。ニューロンでは合成されるATPの実に70%がこの目的に消費されているとも言われています。その結果、上の図のように、細胞内K+イオン濃度は高く、外では低くなり、Na+はこの逆、というイオン環境が作られます。そして細胞膜にはもう一つ重要な性質があります。普段、K+イオンは細胞膜を自由に通れるけれどNa+イオンはそうではない、という事です。これには細胞膜のK2Pチャネルと呼ばれる蛋白質などが関与していると考えられています。この結果、熱力学的には、K+イオン濃度が均一になる方向、即ち、細胞の内から外にイオンが拡散する力が生まれます(緑矢印)。ところが、このようなK+イオンの移動が起こると、電荷バランスが崩れるために細胞内は外に比べて負の電位になります。つまり電気的には、K+イオンは細胞内に向かう方向(赤色)に力を受けるようになります。この熱力学的(エントロピックな)効果と、拮抗する静電的な効果が釣り合うところが平衡状態となります。定量的には、ネルンスト(W. H. Nernst)により定式化されています。ちなみに、このような非対称的なイオン環境を実感できるもっとも簡単な実験は、指先の“ささくれ”のような小さな傷にNaClとKClの水溶液を一滴ずつ垂らしてみる事です。KCl水溶液のほうがより“しみる”はずです。「傷口に塩をぬる」ということわざがありますが、「塩」とは、きっと「カリウム塩」に違いありません・・・。
Action Potential
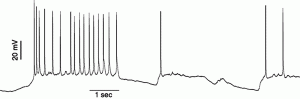
ニューロンや筋の細胞などでは、ある外部入力で膜電位が正の方向に変動すると、Na+イオンが膜を少し通れるようになります。これは細胞膜にあって普段は閉じていた電位依存性Na+チャネルが一部、開くためです。すると状況が一変します。Na+イオンが細胞内に流入する事で膜電位が正に振れさらに多くのNa+チャネルが開く、という増幅過程が起こります。こうして膜電位は極めて短時間に(サブミリ秒)に+50mV以上に達します。引き続いてNa+チャネルの不活性化とK+イオン透過性の上昇が起きる為に、膜電位は再び負に戻されます。その結果スパイク状の電気信号が発生します。このスパイクはaction potential (活動電位)と呼ばれ、生体電気信号の本質的な構成要素です。さきほどのささくれの例では、傷口周辺の感覚細胞でこの活動電位が発生し、時速約60 Kmで中枢に向かい、痛みとして認識されていたのです。下は海馬培養ニューロンからガラス電極を用いて記録されたaction potential の列です。
電気→化学→電気 ・・・
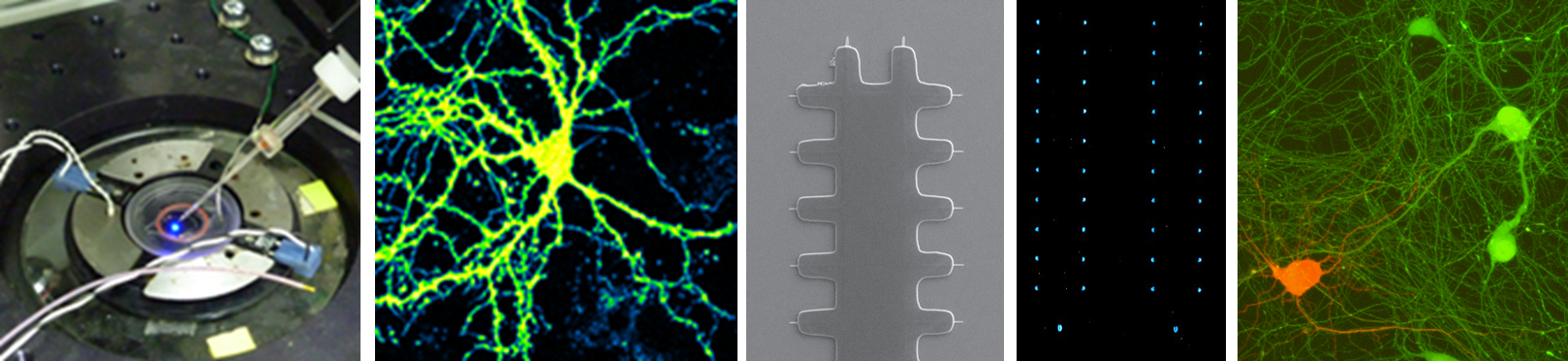
活動電位がニューロンの末端のシナプスと呼ばれる場所に到着するとトランスミッターとよばれる化学物質が放出され、化学信号の形で次のニューロンに出力します。そしてこの信号伝達の効率は時間と共に、そして細胞の活動履歴などに応じてダイナミックに変化する事が知られています。そしてこのような変化こそが、我々が何かを覚えたり、忘れてしまったりする事の素過程ではないかと考えられるようになっています。 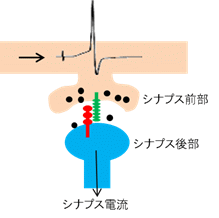 このような興奮性細胞やそれらが作るネットワークの活動の読み取り技術の構築に、大きく分けて二つのアプローチで取り組んでいます。光学的手法と、微細加工技術に基づく新しい細胞活動の読み取り技術です。
このような興奮性細胞やそれらが作るネットワークの活動の読み取り技術の構築に、大きく分けて二つのアプローチで取り組んでいます。光学的手法と、微細加工技術に基づく新しい細胞活動の読み取り技術です。
555