研究活動の検索
研究概要(研究室ガイド)やプレスリリース・受賞・イベント情報など、マテリアルサイエンスの研究室により公開された情報の中から、興味のある情報をタグや検索機能を使って探すことができます。科学技術振興機構のさくらサイエンスプログラムを実施
物質化学フロンティア研究領域の長尾祐樹教授のマレーシアとの交流計画が科学技術振興機構(JST)の「国際青少年サイエンス交流事業 さくらサイエンスプログラム」に採択されたことを受け、10月5日~10月14日の日程でマレーシア工科大学本校、マレーシア日本国際工科院(MJIIT)、マレーシア工科大学マラッカ校及びマレーシアパハン大学から12名の教員・研究者・大学院生を本学に受け入れました。
「国際青少年サイエンス交流事業 さくらサイエンスプログラム」は、産学官の緊密な連携により、諸外国・地域の青少年を我が国に招へいし、我が国の青少年との科学技術分野の交流を行う事業です。これを通して、
①科学技術イノベーションに貢献しうる優秀な人材の養成・確保
②国際的頭脳循環の促進
③日本と諸外国・地域の教育研究機関間の継続的連携・協力・交流
④科学技術外交にも資する日本と諸外国・地域との友好関係の強化
に貢献し、ひいては、日本及び世界の科学技術・イノベーションの発展に寄与することを目的とします。
参考:https://ssp.jst.go.jp/outline/detail/
本学はアジア諸国の大学・研究機関との学術的交流を強く推進しているところであり、将来的に優秀な学生を受け入れるためにマレーシアにおける大学・研究機関においても交流を進めています。
本交流の趣旨はマレーシアの環境・エネルギーに関する技術交流を核に、国際共著論文成果に繋がる大学間連携を強化することができるように計画されました。本学教員による研究指導等を実施し、最終日には成果報告会が行われました。また、金沢のひがし茶屋街での金箔体験や、ゆのくにの森での蒔絵体験を通して日本的な文化や美にも触れ、さらに、東京の日本科学未来館を訪問して日本の多様な先端科学技術を紹介しました。
本交流プログラムはこれらの経験を通して招聘者の将来の日本への留学を促し、本学が招聘者の母国やアジアの科学技術の進歩や発展に貢献することを目指しています。
■実施期間
令和5年10月5日~令和5年10月14日
■研究テーマ
環境・エネルギーに関する技術交流
■本交流について一言
本計画をサポートいただきましたJSTに御礼申し上げます。また、本学受入教員の松見教授、前園教授、西村准教授、本郷准教授、実験や事務手続等をサポートして下さった安准教授をはじめとする10名以上の教職員や学生の皆様に御礼申し上げます。ありがとうございました。引き続きマレーシアとの交流の発展にお力添えをお願い致します。

金沢で金箔体験

ゆのくにの森での蒔絵体験

計算科学チュートリアル

日本科学未来館を訪問
令和5年10月17日
出典:JAIST お知らせ https://www.jaist.ac.jp/whatsnew/info/2023/10/17-1.html電池材料の電極界面ごとの"イオンの流れ"を初めて分離 ―電池材料の性能向上に新たな指針―

  |
北陸先端科学技術大学院大学 東京理科大学 |
電池材料の電極界面ごとの"イオンの流れ"を初めて分離
―電池材料の性能向上に新たな指針―
ポイント
- 電池材料の電極界面ごとに、イオン(プロトン)の流れを分離・定量する手法を開発
- 酸化物界面と金属・炭素界面の輸送特性を定量化することに初めて成功
- 電池材料の性能向上に新たな設計指針を提示し、燃料電池や水電解などの性能向上に貢献
| 北陸先端科学技術大学院大学 物質化学フロンティア研究領域の阿部雄介大学院生(博士前期課程)(研究当時)、青木健太郎助教、Athchaya SUWANSOONTORN研究員(研究当時)、長尾祐樹教授らは、カナダ・カルガリー大学および東京理科大学 創域理工学部の四反田功准教授らとの共同研究により、電池材料の電極を構成する高分子電解質*1薄膜における「イオン(プロトン)」*2輸送を、界面*3ごとに分離・定量する新たな計測手法を開発しました。電池材料の性能向上に新たな指針を与える成果です。 燃料電池や水電解などの電池材料では、電極と高分子電解質が接する「界面」における「プロトン」の流れが性能を大きく左右します。しかし実際の電極では、酸化物、白金、炭素など複数の界面が混在しており、従来の測定ではそれらの輸送が重なって観測されるため、どの界面がどの程度プロトン輸送に寄与しているのか、プロトン伝導度*4を直接測定することができませんでした。このため、電池材料の性能向上に向けた界面設計の指針が得られないという課題がありました。 そこで本研究では、電極構造(くし形のインターディジテッド電極*5)の設計と低周波領域まで拡張したインピーダンス測定*6を組み合わせることで、これまで分離できなかった界面ごとのプロトン輸送を初めて分離・定量する手法を開発しました。その結果、電池材料の電極における酸化物界面と白金・炭素界面で最大で2倍程度異なるプロトン輸送特性を示すことを明らかにし、それぞれの役割を個別に評価できることを実証しました。本成果により、電極界面ごとのプロトン輸送の律速要因を明確に把握することが可能となり、電池材料の選択や界面設計をより合理的に進めることができるようになります。燃料電池に加え、水電解や二次電池、センサなど、さまざまな電気化学デバイスの性能向上に貢献することが期待されます。 |
【研究の背景】
燃料電池や水電解など、次世代エネルギー技術の高効率化に向けて、電極と電解質が接する「界面」におけるプロトンの流れの理解が重要となっています。特に近年、脱炭素社会の実現に向けて、燃料電池や水電解装置の性能向上への期待が高まっており、その鍵を握る界面設計の高度化が求められています。
燃料電池や水電解では、高分子電解質(アイオノマー)が電極表面を覆い、その界面を通じてプロトンが移動しています。しかし、実際の材料では、白金、炭素など複数の界面が混在しており、従来の測定ではそれらすべての寄与が一つに重なって観測されていました。そのため、どの界面でプロトンがどの程度流れているのかを区別することができず、界面設計の指針が得られないという課題がありました。
このように、界面ごとのプロトン輸送を分けて評価する手法が存在しないことが、電極材料や界面構造の最適設計を進める上で大きなボトルネックとなっていました。
【本研究の成果】
本研究では、電極構造(くし形のインターディジテッド電極)の形状を精密に制御するとともに、低周波まで拡張したインピーダンス測定を組み合わせることで、これまで一つに重なって観測されていたプロトン輸送の成分を分離・定量する新たな手法を開発しました。これにより、電極界面ごとのプロトンの流れを個別に評価することに初めて成功しました。その結果、測定信号に含まれる複数の抵抗成分が、それぞれ異なる界面に由来することを明確にし、
・高周波側の抵抗成分は酸化物(SiO2)界面のプロトン伝導
・低周波側の抵抗成分は白金および炭素界面のプロトン伝導
に対応することを明らかにしました。
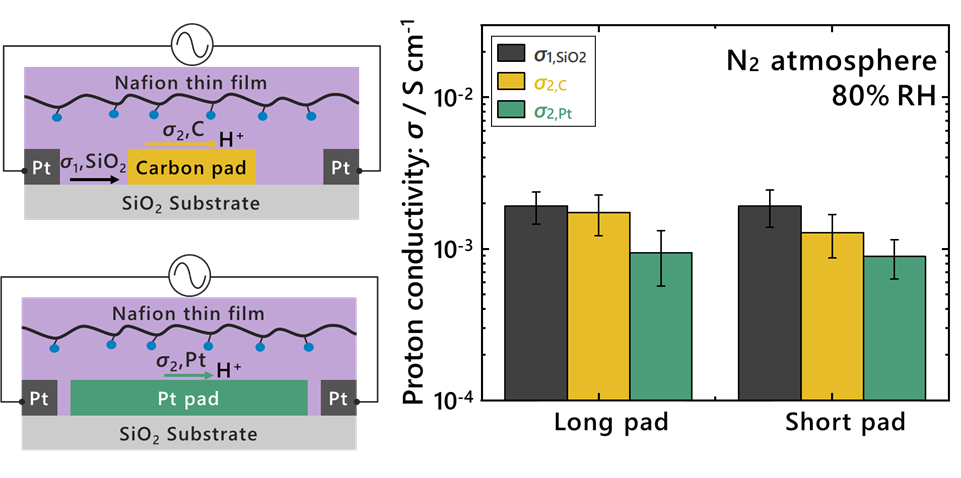
| 図1 本研究の概念図と結果の概要。左図は、ナフィオン薄膜中をプロトンが電極界面に沿って移動する様子を示しています。SiO2基板界面(σ1)と、炭素または白金電極界面(σ2)で異なる輸送経路が存在します。従来はσ2を正確に得ることができていませんでした。右図は、電極パッド長(Long / Short)を変えても、それぞれの界面に対応する伝導度(σ1, σ2)がほぼ一致することを示しています。これは、測定された伝導度が電極構造の影響ではなく界面固有の値であり、σ2が高い精度で定量できていることを示します。 |
さらに、電極パッドの長さを変えても同じ伝導度が得られることから、これらの抵抗成分が電極構造ではなく「界面そのもの」の性質に由来することを実証しました。これにより、従来は一つの値としてしか評価できなかったプロトン伝導度を、界面ごとに分けて定量できることを初めて示しました。
本成果は、これまで"混ざって見えていたプロトンの流れ"を界面ごとに分解して捉えることを可能にした点で、電極界面におけるプロトン輸送の理解を大きく前進させるものです。

| 図2 本研究のまとめ。電池内部では、プロトンが複数の「電極界面」を通って移動していますが、従来はそれらが重なって観測されるため、どこが性能のボトルネックか分かりませんでした。本研究では、櫛のような電極構造を用いてプロトンの流れを界面ごとに「仕分け」して測定することに成功しました。その結果、酸化物と金属・炭素の界面でプロトンの進みやすさが最大で2倍程度異なることを明らかにしました。これにより、電池内部の「渋滞箇所」を特定でき、燃料電池や次世代電池の性能向上に向けた設計が可能になります。(本ポンチ絵は、AIにより作成) |
【社会への還元として期待できる内容、今後の展望】
本研究により、電極と高分子電解質が接する界面におけるプロトン輸送を、界面ごとに分離して評価できる手法が確立されました。これにより、どの界面がイオン輸送のボトルネックとなっているのかを明確に特定できるようになり、電極材料の選択や界面構造の最適化を、従来よりも科学的根拠に基づいて設計することが可能となります。特に、燃料電池や水電解装置の開発においては、エネルギー変換効率の向上やコスト低減が重要な課題であり、本手法はその設計指針を与える基盤技術として、材料開発やデバイス設計に直接的に貢献することが期待されます。また、本手法は、燃料電池に限らず、水電解、二次電池、センサなど、電極界面でのイオン輸送が重要となるさまざまな電気化学デバイスに適用可能であり、それらの性能向上に貢献すると考えられます。
今後は、実際の複雑な電極構造への展開や、界面構造とイオン輸送の関係の解明を進め、より高効率で高機能なエネルギー・デバイスの実現を目指します。
本研究は、国立研究開発法人科学技術振興機構(JST) 戦略的創造研究推進事業CREST(JPMJCR21B3)、日本学術振興会(JSPS) 科研費 新学術研究領域「ハイドロジェノミクス」(JP21H00020)、公益財団法人 村田学術振興・教育財団 研究助成による財政的支援を受けて実施されました。
【論文情報】
| 掲載誌 | ACS Applied Materials & Interfaces |
| 論文タイトル | Decoupling Interfacial Proton Conductivity in Ionomer Thin Films on Pt and Carbon Electrodes |
| 著者 | Yusuke Abe, Kentaro Aoki, Athchaya Suwansoontorn, Kunal Karan, Isao Shitanda, Yuki Nagao* |
| 掲載日 | 2026年5月1日 |
| DOI | 10.1021/acsami.6c04425 |
【用語説明】
イオンを運ぶ機能を持つ高分子材料です。燃料電池などでは、プロトン*2を選択的に輸送する役割を担います。本研究では代表的な高分子電解質であるナフィオンを使用しています。ナフィオンは、プロトンを効率よく輸送できるため、燃料電池などで広く利用されています。
水素原子が電子を失った粒子(H+)で、電気を運ぶ役割を持つイオンです。燃料電池や水電解などは、このプロトンを電子と別々に流すことで動きます。
異なる材料が接している境界のことです。本研究では、ナフィオンとSiO2(酸化物)、白金、炭素との接触部分を指します。
プロトンがどれだけ流れやすいかを表す指標です。値が大きいほど、プロトンが移動しやすいことを意味します。
櫛(くし)の歯のように電極が交互に並んだ構造を持つ電極です。電極間を横方向に流れるイオンの動きを測定するのに適しています。
交流電圧を加えて材料の応答を調べる測定手法で、イオンの動きや電気的な抵抗を周波数ごとに解析することができます。
令和8年5月11日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2026/05/11-1.html多剤耐性がんを克服する新たなナノ粒子薬物送達システムの開発に成功 ―アミノ酸由来のナノ粒子による逐次的薬物放出と光熱療法の融合ー
  |
国立大学法人東北大学 国立大学法人北陸先端科学技術大学院大学 |
多剤耐性がんを克服する新たなナノ粒子薬物送達システムの開発に成功
―アミノ酸由来のナノ粒子による逐次的薬物放出と光熱療法の融合―
【発表のポイント】
- アミノ酸を原料とした超微小粒子(ナノ粒子(注1))を独自の製法で作製し、抗がん剤をより多く効率よく詰め込むことに成功しました。
- 粒子の表面加工により、がん細胞が抗がん剤を細胞の外へ追い出す前に、その「排出ポンプ」の働きをあらかじめ止めてから抗がん剤を届ける仕組みを実現しました。
- 薬による治療とレーザー光を使った熱治療を組み合わせることで、治療が難しい多剤耐性がんのマウス実験において、40日間すべてのマウスが生存するという顕著な効果を達成しました。
- 開発したナノ粒子は正常な組織への毒性がなく、がん細胞を狙い撃ちにする機能も確認されました。
【概要】
| がん細胞が、複数の抗がん剤に対して同時に抵抗性を持つようになる現象「多剤耐性」は、がんに対する化学療法において大きな課題となっています。 東北大学 多元物質科学研究所の都英次郎教授(北陸先端科学技術大学院大学 先端科学技術研究科 客員教授)らの研究グループは、多剤耐性(注2)がんの治療に向けた革新的なナノ粒子薬物送達システムの開発に成功しました(図1)。本研究グループは、アミノ酸を原料とした超微小粒子(ナノ粒子)を独自の製法で作製し、その表面をイカやタコの墨に含まれる色素に似た物質(ポリドーパミン(注3))で層状にコーティングしました。この加工により、多剤耐性がん細胞が抗がん剤を排出する前に細胞内に蓄積させることが可能となりました。さらに、腫瘍部位を局所的に加熱する光熱療法との組み合わせにより、マウス実験で治療開始からわずか7日で腫瘍が完全に消失し、40日間すべてのマウスが副作用なく生存しました。 本成果は多剤耐性がんに対する化学療法と光熱療法を融合した新しい治療戦略として、高い臨床応用可能性を持ち、今後、様々な種類の多剤耐性腫瘍への応用拡大が期待されます。 本研究成果は、薬物送達分野の国際的権威ある学術誌「Journal of Controlled Release」に、2026年5月6日付けで掲載されました。 なお、本研究はフランス国立科学研究センター(CNRS)ストラスブール大学のAlberto Bianco博士、Cécilia Ménard-Moyon博士らの研究グループとの共同研究によるものです。 |
【詳細な説明】
研究の背景
がん化学療法における最大の障壁の一つが多剤耐性(MDR)の発現です。MDRを獲得したがん細胞は、細胞膜上にP糖タンパク質(P-gp)(注4)と呼ばれる薬物排出ポンプを過剰発現させ、投与された抗がん剤を細胞外へ積極的に排出してしまいます。その結果、薬剤の細胞内濃度が著しく低下し、治療効果が大幅に損なわれます。この問題を解決するため、P-gp阻害剤と抗がん剤を同時に投与する手法が検討されてきましたが、両薬剤が同時に放出されると、P-gpの阻害が完了する前に抗がん剤が排出されてしまうという課題がありました。
今回の取り組み
本研究グループは、チロシンおよびトリプトファンのアミノ酸誘導体を自己集合・紫外線架橋させたナノ粒子を出発材料として、独自の自己鋳型エッチング法によって多孔質アミノ酸ナノ粒子(CPP)を作製しました。この多孔質構造により、抗がん剤ドキソルビシン(Dox)(注5)を従来の非多孔質ナノ粒子(積載効率~15%、封入効率~57%)と比べて大幅に高効率で担持することが可能となりました。
次に、ナノ粒子表面にポリドーパミン(PDA)を層ごとに積層コーティングし、さらにP-gp阻害剤であるキニジン(注6)をpH感受性のイミン結合を介して表面に結合させました。この設計により、以下の3つの革新的な機能が実現されました。
1つは、逐次的薬物放出(注7)です。酸性・グルタチオン(GSH)豊富な腫瘍細胞内環境に応答して、キニジンがDoxより先に放出されます。PDAコーティング層数を3層とすることで、キニジンがP-gpを阻害した後にDoxが放出される最適な逐次放出プロファイルを実現しました。
2つ目は、光熱療法(PTT)(注8)です。PDAコーティングは近赤外線(808 nm)を吸収して熱に変換する優れた光熱変換能を示し、腫瘍部位における温度を51℃まで上昇させることが確認されました。
3つ目は、腫瘍ターゲティングです。PEGリンカーを介して表面に結合させた葉酸(FA)(注9)が、多くの腫瘍細胞で過剰発現している葉酸受容体を標的とし、ナノ粒子の腫瘍への選択的集積を促進しました。
多剤耐性EMT-6/AR1細胞を用いたin vitro実験において、本ナノ粒子(FA/C-Dox@PDA-Q)とレーザー照射を組み合わせた治療により、細胞生存率が5%未満にまで低下することが確認されました。これは化学療法単独やPTT単独の効果をはるかに超えるものです。
多剤耐性EMT-6/AR1腫瘍を移植したマウスモデルを用いたin vivo実験では、FA/C-Dox@PDA-Q+レーザー照射群において、治療開始7日後に腫瘍の完全消退が観察され、40日間の観察期間中に100%の生存率が達成されました(図2)。一方、薬剤を含まないナノ粒子(PTT単独)の群では一時的な腫瘍消退後に再発が認められ(40日生存率20%)、その他の対照群はすべて生存率0%でした。血液検査および体重モニタリングの結果から、本ナノ粒子の全身毒性がないことも確認されました。
今後の展開
本研究で開発したナノ粒子プラットフォームは、多剤耐性がんに対する化学療法と光熱療法を融合した新しい治療戦略として、高い臨床応用可能性を持ちます。今後は、様々な種類の多剤耐性腫瘍への応用拡大や、さらなる安全性・有効性の検討を進めていく予定です。

図1. 本研究の概念
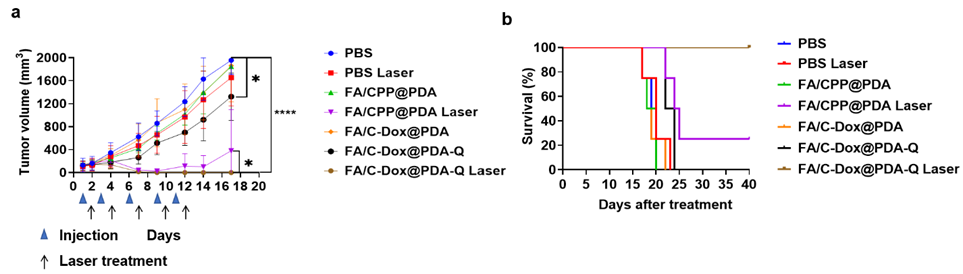
| 図2. マウスを用いた抗腫瘍効果の検証 (a) 腫瘍の大きさの変化(治療開始からの日数)4種類の条件でマウスに投与し、腫瘍の大きさを継続的に観察しました。機能性ナノ粒子(FA/C-Dox@PDA-Q)と近赤外線レーザー照射を組み合わせた群では、わずか7日間で腫瘍が完全に消失しました。一方、薬剤を含まないナノ粒子+レーザー照射の群では一時的な腫瘍消失の後に再増殖が認められ、それ以外の対照群では腫瘍の抑制効果はほとんど見られませんでした。▲印はナノ粒子の投与日、↑印はレーザー照射日を示します。 (b) 生存率(治療開始から40日間)機能性ナノ粒子(FA/C-Dox@PDA-Q)+レーザー照射を受けたすべてのマウスが、観察期間の40日間を通じて生存しました(生存率100%)。一方、他の治療条件のマウスはいずれも40日以内に全例死亡しており、本治療法の顕著な生存延長効果が示されました。 |
【謝辞】
本研究は、フランス国立科学研究センター(CNRS)、フランス国立研究機構(ANR)LabExプロジェクト(ANR-10-LABX-0026_CSC)、Jean-Marie Lehn財団、JSPS科研費 基盤研究(A)(JP23H00551)、挑戦的研究(開拓)(JP22K18440、JP25K21827)、地域中核・特色ある研究大学強化促進事業(JPMJTR22U1)、JST共創の場形成支援プログラムJPMJSF2318の支援を受けて実施されました。
【用語説明】
【論文情報】
| タイトル | Multifunctional amino acid-based nanoparticles for sequential drug delivery to overcome multidrug resistant cancer |
| 著者 | Tengfei Wang, Nina Sang, Cécilia Ménard-Moyon,* Eijiro Miyako,* Alberto Bianco* *責任著者:東北大学多元物質科学研究所 教授 都英次郎 フランス国立科学研究センター(CNRS)ストラスブール大学 Alberto Bianco博士、Cécilia Ménard-Moyon博士 |
| 掲載誌 | Journal of Controlled Release |
| DOI | 10.1016/j.jconrel.2026.114954 |
| URL | https://doi.org/10.1016/j.jconrel.2026.114954 |
令和8年5月8日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2026/05/08-1.html両生類・爬虫類の腸内細菌から画期的ながん治療細菌を発見!
両生類・爬虫類の腸内細菌から画期的ながん治療細菌を発見!
【ポイント】
- 両生類・爬虫類の腸内から採取した天然細菌が、一度限りの投与でがん組織を完全に消失させることを実証
- 細菌による直接的ながん細胞殺傷と、免疫系の活性化による間接的攻撃の両方を実現
- 既存の化学療法や免疫療法を上回る治療効果を示しながら、正常組織への悪影響なし
- 多様な固形がんへの適用が期待され、新たながん治療法開発への道を拓く
| 北陸先端科学技術大学院大学 物質化学フロンティア研究領域の都 英次郎教授の研究チームは、ニホンアマガエル(Dryophytes japonicus)、アカハライモリ(Cynops pyrrhogaster)、カナヘビ(Takydromus tachydromoides)の腸内から計45株の細菌を単離しました。これらの細菌を系統的にスクリーニングした結果、9株が抗腫瘍効果を示し、中でもニホンアマガエルの腸内から単離した細菌Ewingella americanaが、マウスのがんモデルで一度限りの投与により腫瘍を完全に消失させる極めて強力な抗がん作用を持つことを発見しました。 近年、腸内細菌とがんの関係が注目されていますが、これまでは主に腸内細菌叢全体の調整や糞便移植などの間接的アプローチが中心でした。本研究では、これとは全く異なるアプローチとして、腸内細菌を単離・培養し、直接静脈投与することで、がんを直接攻撃する革新的な治療法を開発しました。 本研究成果は、国際学術誌Gut Microbesに掲載されました。 |
【研究の詳細】
・驚異的な治療効果
マウスを用いた大腸がんモデルにおいて、E. americanaをたった一回静脈投与するだけで、腫瘍が完全に消失し、100%の完全奏効[注1]率(CR率)を達成しました(図1)。これは、現在標準治療として使われている免疫チェックポイント阻害薬[注2](抗PD-L1抗体)やリポソーム化ドキソルビシン(化学療法剤)を大きく上回る治療効果です。
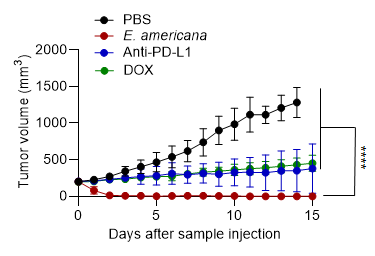
図1. 抗がん効果:Ewingella americanaと従来治療法との比較
| 腫瘍応答:E. americana単回静脈内投与(200 µL、5 × 10⁹ CFU/mL)、ドキソルビシン(DOX)または抗PD-L1抗体4回投与(200 µL、2.5 mg/kg/回)、PBSを対照として使用。データ:平均値 ± 標準誤差(n = 5)。****、p < 0.0001(スチューデントの両側 t 検定) |
・二重作用による抗がん効果
E. americanaは以下の二つのメカニズムでがんを攻撃します(図2)。
- 直接的殺傷効果:
通性嫌気性細菌[注3] であるE. americanaは、低酸素状態のがん組織に選択的に集積し、がん細胞を直接破壊します。腫瘍内での細菌数は投与後24時間で約3,000倍に増加し、効率的にがん組織を攻撃します。 - 免疫活性化効果:
細菌の存在が免疫系を強力に刺激し、T細胞、B細胞、好中球などの免疫細胞ががん組織に集結します。これらの免疫細胞が産生する炎症性サイトカイン(TNF-α、IFN-γ)がさらに免疫応答を増幅し、がん細胞のアポトーシス(細胞死)を誘導します。

図2. Ewingella americanaの抗腫瘍メカニズム
・腫瘍特異的な集積メカニズム
E. americanaは、がん組織に選択的に集積し、正常組織には全く定着しません。この驚くべき腫瘍特異性は、以下の複合的メカニズムによるものと考えられます。
- 低酸素環境:がん組織特有の低酸素状態が嫌気性細菌の増殖を促進
- 免疫抑制環境:がん細胞が発現するCD47[注4]タンパク質により局所的免疫抑制が生じ、細菌が生存しやすい環境を形成
- 異常血管構造:がん組織の血管は穴が多く、細菌が容易に侵入できる
- 代謝異常:がん特有の代謝産物が細菌の選択的増殖を支援
・優れた安全性プロファイル
詳細な安全性評価により、E. americanaは以下の特徴を示しました。
- 血中から急速に除去(半減期約1.2時間、24時間後には完全に検出不能)
- 肝臓、脾臓、肺、腎臓、心臓などの正常臓器に細菌の定着は一切なし
- 一過性の軽度炎症反応のみで、72時間以内に正常化
- 60日間の長期観察でも慢性毒性なし
【今後の展開】
本研究により、天然細菌を用いた新しいがん治療法の可能性が実証されました。今後は以下の研究開発を進める予定です。
- 他のがん種への適用拡大:乳がん、膵臓がん、メラノーマなど、多様ながん種での効果検証
- 投与方法の最適化:分割投与、腫瘍内投与など、より安全で効果的な投与法の開発
- 併用療法の開発:既存の免疫療法や化学療法との組み合わせによる相乗効果の検証
本研究は、未開拓の生物多様性が新たな医療技術開発の宝庫であることを示すとともに、難治性がん患者に新たな治療選択肢を提供する可能性を秘めています。
【用語解説】
治療により腫瘍が完全に消失し、検査で確認できなくなった状態。
がん細胞による免疫抑制を解除し、T細胞ががん細胞を攻撃できるようにする薬剤。
酸素がある環境でも無い環境でも増殖できる細菌。がん組織の低酸素領域で選択的に増殖できる。
細胞表面に発現する「食べないで」信号を出すタンパク質。がん細胞はこれを過剰発現して免疫細胞による攻撃を回避する。
【論文情報】
| 掲載誌 | Gut Microbes |
| タイトル | Discovery and characterization of antitumor gut microbiota from amphibians and reptiles: Ewingella americana as a novel therapeutic agent with dual cytotoxic and immunomodulatory properties |
| 著者 | Seigo Iwata, Nagi Yamasita, Kensuke Asukabe, Matomo Sakari, Eijiro Miyako* |
| 掲載日 | 2025年12月10日 |
| DOI | 10.1080/19490976.2025.2599562 |
【研究資金】
本研究は、以下の研究資金の支援を受けて実施されました。
日本学術振興会(JSPS)科学研究費助成事業 基盤研究(A)(課題番号:23H00551)
同 科学研究費助成事業 挑戦的研究(開拓)(課題番号:22K18440)
同 地域中核・特色ある研究大学強化促進事業(課題番号:JPJS00420230006)
科学技術振興機構(JST)共創の場形成支援プログラム(課題番号:JPMJSF2318)
同 次世代研究者挑戦的研究プログラム(SPRING)(課題番号:JPMJSP2102)
令和7年12月15日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2025/12/15-1.html海洋細菌による新しいがん免疫療法の開発に成功! ~遺伝子改変不要の天然細菌が大腸がんを選択的に攻撃~
海洋細菌による新しいがん免疫療法の開発に成功!
~遺伝子改変不要の天然細菌が大腸がんを選択的に攻撃~
【ポイント】
- 海洋細菌Photobacterium angustumが大腸がんに対して強力な抗腫瘍効果を示すことを世界で初めて発見
- 遺伝子改変を一切行わない天然細菌でありながら、がん組織に選択的に集積し、健康な臓器への影響が極めて少ない
- 細菌による直接的ながん細胞破壊と免疫系の活性化という二つのメカニズムで腫瘍を攻撃
- 従来の細菌療法と比較して優れた治療効果と安全性を確認
| 北陸先端科学技術大学院大学 物質化学フロンティア研究領域の都 英次郎教授と宮原 弥夏子大学院生(博士後期課程、JAIST SPRING研究員)らの研究チームは、海洋細菌*1Photobacterium angustum(フォトバクテリウム・アングスタム)が大腸がんに対して顕著な治療効果を示すことを発見しました。 本研究では、複数の海洋細菌株をスクリーニングした結果、P. angustumが遺伝子改変を施さない天然の状態で、がん組織に選択的に集積し、直接的な腫瘍溶解作用と強力な免疫活性化を引き起こすことを明らかにしました。マウスモデルにおいて、静脈内投与されたP. angustumは腫瘍組織に高度に集積する一方、肝臓を除く重要臓器への定着はほとんど認められず、血液学的異常や組織学的毒性も観察されませんでした。 さらに、P. angustumによる治療は、T細胞、B細胞、好中球などの免疫細胞の腫瘍内浸潤を促進し、腫瘍壊死因子α(TNF-α)やインターフェロンγ(IFN-γ)などの炎症性サイトカイン*2の産生を増強しました。また、細菌が産生する天然の外毒素*3により、がん細胞を直接破壊する能力も確認されました。これらの複合的な作用により、治療を受けたマウスの生存期間が著しく延長し、一部の個体では完全寛解が達成されました。 本研究成果は、遺伝子組み換え生物(GMO)*4に依存しない、より安全で生体適合性の高い新しいがん免疫療法の開発につながる重要な知見です。 この研究の詳細は、がん免疫療法分野の国際的トップジャーナルである「Journal for ImmunoTherapy of Cancer」に掲載されました。 |
【研究背景と内容】
がんは世界的な死因の上位を占めており、免疫チェックポイント阻害剤やCAR-T細胞療法などの画期的な免疫療法が開発されてきました。しかし、これらの治療法は高額であり、免疫関連の副作用、固形腫瘍における限定的な効果、腫瘍微小環境*5における免疫抑制機構などの課題があります。
細菌を用いたがん治療は150年以上前から検討されてきましたが、近年、特定の細菌種が腫瘍の低酸素環境や免疫抑制環境に選択的に定着し増殖する能力を持つことが明らかになり、注目を集めています。しかし、これまでの研究の多くは遺伝子改変された大腸菌やサルモネラ菌を用いており、安全性の懸念、複雑な製造プロセス、厳格な規制などの課題がありました。
本研究では、遺伝子改変を行わない天然の海洋細菌に着目し、がん治療への応用可能性を探索しました。
【研究の内容】
1. 海洋細菌のスクリーニング
研究グループは、P. angustum、P. phosphoreum、P. aquimaris、A. logei、P. indicumを含む複数の海洋細菌株について、大腸がんマウスモデルにおける抗腫瘍活性を評価しました。その結果、P. angustumのみが顕著な抗腫瘍効果を示し(図1)、生存期間を著しく延長させました。他の細菌株は高い毒性により投与後2日以内にマウスが死亡しました。
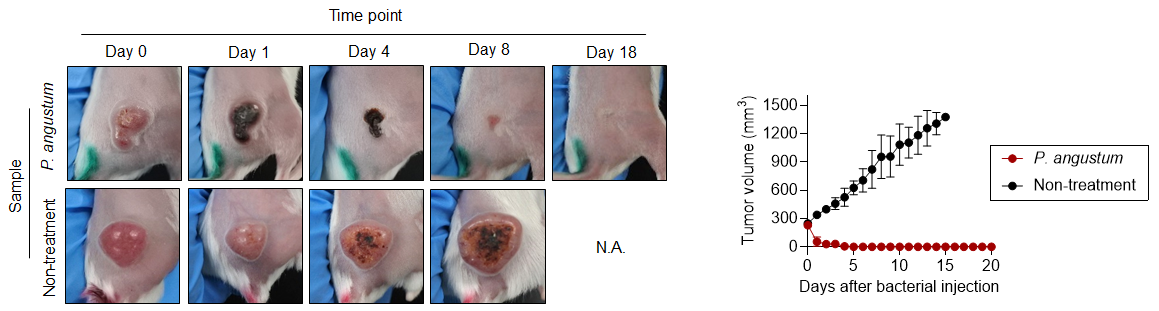
図1. 大腸がんマウスモデルにおけるP. angustumの抗腫瘍活性
2. 優れた安全性プロファイル
P. angustum投与後のマウスにおいて、体重減少や血液学的異常は認められませんでした。完全血球計算、生化学的分析、組織学的検査のいずれにおいても、毒性の徴候は観察されませんでした。また、炎症性サイトカインの上昇は毒性株と比較して顕著に低く、24時間後には肝臓を除く重要臓器から細菌が検出されませんでした。
3. 高い腫瘍選択性
静脈内投与されたP. angustumは、腫瘍組織に選択的に集積し、多数のコロニー形成が確認されました。一方、心臓、肺、腎臓、脾臓などの健康な臓器への定着はほとんど認められませんでした。
4. 二重の抗腫瘍メカニズム
P. angustumの抗腫瘍効果は、以下の二つのメカニズムによるものと考えられます(図2):
- 直接的な腫瘍溶解作用:細菌が産生する天然の外毒素(ヘモリシンなど)により、がん細胞を直接破壊
- 免疫系の活性化:T細胞、B細胞、好中球の腫瘍内浸潤を促進し、TNF-αやIFN-γなどの炎症性サイトカインの産生を増強
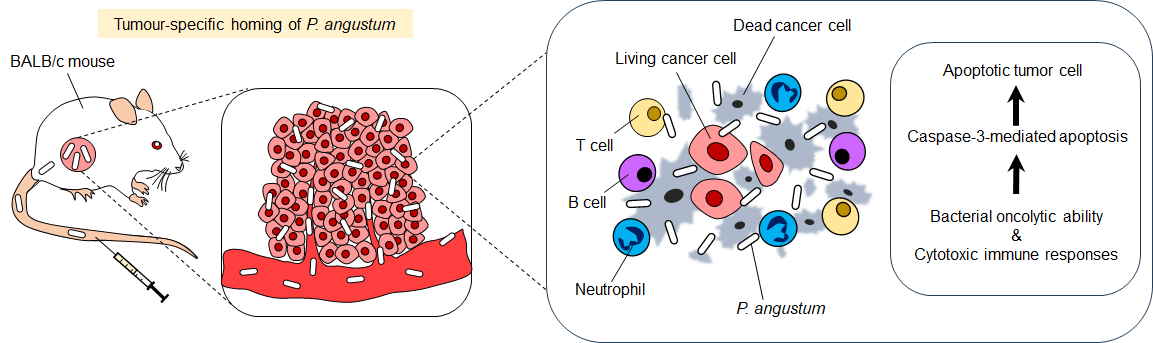
図2. P. angustumによる抗腫瘍メカニズム
5. 幅広い適用可能性
P. angustumは、炎症誘発性の大腸がんモデルに加え、薬剤耐性のトリプルネガティブ乳がんモデルにおいても顕著な抗腫瘍効果を示しました。これは、本治療法が大腸がん以外のがん種にも応用できる可能性を示唆しています。
【研究の意義と今後の展望】
本研究は、遺伝子改変を必要としない天然細菌が、安全かつ効果的ながん免疫療法として機能することを実証しました。今後は、さまざまながん種での有効性の検証、免疫チェックポイント阻害剤との併用効果の評価、長期的な免疫記憶の詳細な解析などを進める予定です。
また、P. angustumの腫瘍選択的な定着メカニズムや免疫活性化の分子機構をさらに解明することで、より効果的な治療法の開発につながることが期待されます。
本研究成果は、GMOに依存しない生体適合性の高い細菌療法という新しい治療パラダイムを提示するものであり、将来的には臨床応用に向けた開発が期待されます。
【研究支援】
本研究は、以下の研究資金の支援を受けて実施されました:
日本学術振興会(JSPS)科学研究費助成事業 基盤研究(A)(課題番号:23H00551)
同 科学研究費助成事業 挑戦的研究(開拓)(課題番号:22K18440)
同 地域中核・特色ある研究大学強化促進事業(課題番号:JPJS00420230006)
科学技術振興機構(JST)共創の場形成支援プログラム(課題番号:JPMJSF2318)
同 次世代研究者挑戦的研究プログラム(SPRING)(課題番号:JPMJSP2102)
【論文情報】
| 掲載誌 | Journal for ImmunoTherapy of Cancer |
| 論文題目 | Systemic administration of Photobacterium angustum promotes antitumor immunity and direct tumor lysis in murine models of colorectal cancer |
| 著者 | Mikako Miyahara, Teruhisa Takizawa, Matomo Sakari, Eijiro Miyako* |
| 掲載日 | 2025年11月19日にオンライン版に掲載 |
| DOI | 10.1136/jitc-2025-012665 |
【用語説明】
海洋環境に生息する細菌の総称。本研究で使用したPhotobacterium angustumは、特殊な培養条件を必要とせず、通常の海洋培地で培養可能。
細胞間の情報伝達に関与するタンパク質。TNF-αやIFN-γは免疫応答を促進する炎症性サイトカイン。
細菌が体外に分泌する毒性物質。本研究では、P. angustumが産生する外毒素ががん細胞を直接破壊することが示された。
遺伝子工学的手法により遺伝子を改変した生物。本研究で使用したP. angustumは天然株であり、遺伝子改変は行っていない。
がん組織とその周辺の細胞、血管、免疫細胞、シグナル分子などから構成される環境。多くの場合、低酸素状態や免疫抑制状態にある。
令和7年11月21日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2025/11/21-1.html物質化学フロンティア研究領域の都教授がBioJapan 2025 NINEJP「ピッチ&マッチングカンファレンス」研究シーズ部門において最優秀賞を受賞
物質化学フロンティア研究領域の都英次郎教授が、北陸地域の大学等発スタートアップ支援拠点Tech Startup HOKURIKU(TeSH)の代表としてBioJapan 2025 NINEJP「ピッチ&マッチングカンファレンス」に登壇し、研究シーズ部門において最優秀賞(Best Academic Seed Award)を受賞しました。
BioJapan 2025 NINEJP「ピッチ&マッチングカンファレンス」は、令和7年10月10日にパシフィコ横浜で開催された、NINEJPが主催する公式ピッチセッションです。全国9つのプラットフォームから推薦されたバイオ分野の革新的な研究者と有望な大学発スタートアップが研究成果と事業化構想を発表し、技術的独創性と将来性を競い合いました。
NINEJPは、JSTの「大学発新産業創出基金事業(全国ネットワーク構築支援)」の一環として設立された、全国9つの大学等発スタートアップ・プラットフォームが連携するイノベーション・エコシステムです。日本全体でグローバルに通用するディープテック事業を創出することを目的としています。
※参考:BioJapan 2025
NINEJP
Tech Startup HOKURIKU(TeSH)
■受賞年月日
令和7年10月10日
■発表テーマ
高い安全性と強力な抗腫瘍効果を併せ持つ腫瘍内細菌コンソーシアムを用いた次世代型がん細菌療法
(Nature's Own Bacterial Consortium: A Gene-Free,Safe,and Powerful Cancer Therapy)
■発表者
都英次郎
■受賞対象となった研究の内容
「Nature's Own Bacterial Consortium: A Gene-Free, Safe, and Powerful Cancer Therapy」 と題した発表を行い、遺伝子改変を必要としない天然細菌コンソーシアム AUN による革新的ながん細菌療法について紹介しました。
本技術は、高い安全性と免疫非依存的な抗腫瘍効果を両立させる全く新しい治療モダリティとして、審査委員より、その科学的独創性と臨床応用の可能性が高く評価され、最優秀賞の受賞に至りました。
■受賞にあたって一言
この受賞は、北陸地域発の研究シーズが全国レベルで高く評価された成果であり、TeSHおよび本学が推進するアカデミア創薬・ディープテック領域の強みを示すものです。
JAISTおよびTeSHでは、今後も地域発の優れたシーズを発掘・育成し、グローバルに展開可能なスタートアップ創出を目指して取り組んでまいります。


令和7年11月11日
出典:JAIST 受賞https://www.jaist.ac.jp/whatsnew/award/2025/11/11-1.htmlリチウムイオン電池の劣化原因をナノスケールで可視化 ― 新手法「ケプストラム照合解析」で電池現象の解明に貢献 ―
  |
北陸先端科学技術大学院大学 東京科学大学 |
リチウムイオン電池の劣化原因をナノスケールで可視化
― 新手法「ケプストラム照合解析」で電池現象の解明に貢献 ―
【ポイント】
- リチウムイオン電池の劣化につながる正極の結晶構造変化をナノメートルスケールで可視化
- 新開発の「ケプストラム照合解析」により、高空間分解能・広視野・低損傷を同時に実現
- 電池劣化の原因となる界面での構造変化を解明し、高性能電池開発への貢献に期待
| 北陸先端科学技術大学院大学 ナノマテリアル・デバイス研究領域の麻生浩平講師、掛谷尚史大学院生(博士後期課程)、土田拓夢大学院生(博士前期課程)、大島義文教授、東京科学大学 物質理工学院応用化学系の伊藤広貴大学院生(博士前期課程)(研究当時)、淺野翔大学院生(博士後期課程)(研究当時)、渡邊健太助教、平山雅章教授、物質・材料研究機構 マテリアル基盤研究センターの三石和貴副センター長、木本浩司センター長、蓄電池基盤プラットフォームの篠田啓介エンジニア、エネルギー・環境材料研究センターの増田卓也センター長の研究グループは、リチウムイオン電池の結晶構造変化をナノメートル (nm:10億分の1メートル)スケールで可視化する新手法「ケプストラム照合解析」を確立しました。 新手法によって、従来の分析手法では困難だった、高空間分解能(約1 nm)・広視野(数百nm)・試料低損傷の三点を同時に実現しました。そして、この手法をエピタキシャル薄膜*1として作製したコバルト酸リチウム(LiCoO2)正極に応用することで、電解質との界面付近において、電池劣化の原因となるナノスケールの構造変化を可視化することに成功しました。今回、開発された手法は、電池における構造変化の理解を加速することで、電池の劣化原因解明や高性能化に役立つと期待されます。 本研究成果は、2025年10月21日(米国東部標準時間)に科学雑誌「Nano Letters」誌のオンライン版で公開されました。 |
【研究概要】
スマートフォンや電気自動車にはリチウムイオン電池(LIB)が欠かせません。その正極として広く用いられている材料が、層状の結晶構造(原子の並び方)を有するリチウム遷移金属酸化物(以下、層状正極)です。LIBの長時間稼働を実現するには、より高電圧で動かすことが重要となります。一方、高電圧で充放電を繰り返すと、液体電解質と接する界面において、層状正極がスピネル構造や岩塩構造*2に変化して、LIBの劣化を引き起こします。界面を起点として数nm のスケールで進行する構造変化を理解するために、解析が求められてきました。
従来の光やX線を使った観察では、空間分解能が数十〜数百nmに限られます。電子顕微鏡なら原子スケールで観察できますが、観察視野が約50×50 nm2に制限される課題と、多量の電子照射によって観察中に試料が損傷する課題がありました。つまり、「ナノ空間分解能」「広視野」「低試料損傷」の三つを両立して、層状正極の構造を解析できる手法がありませんでした。
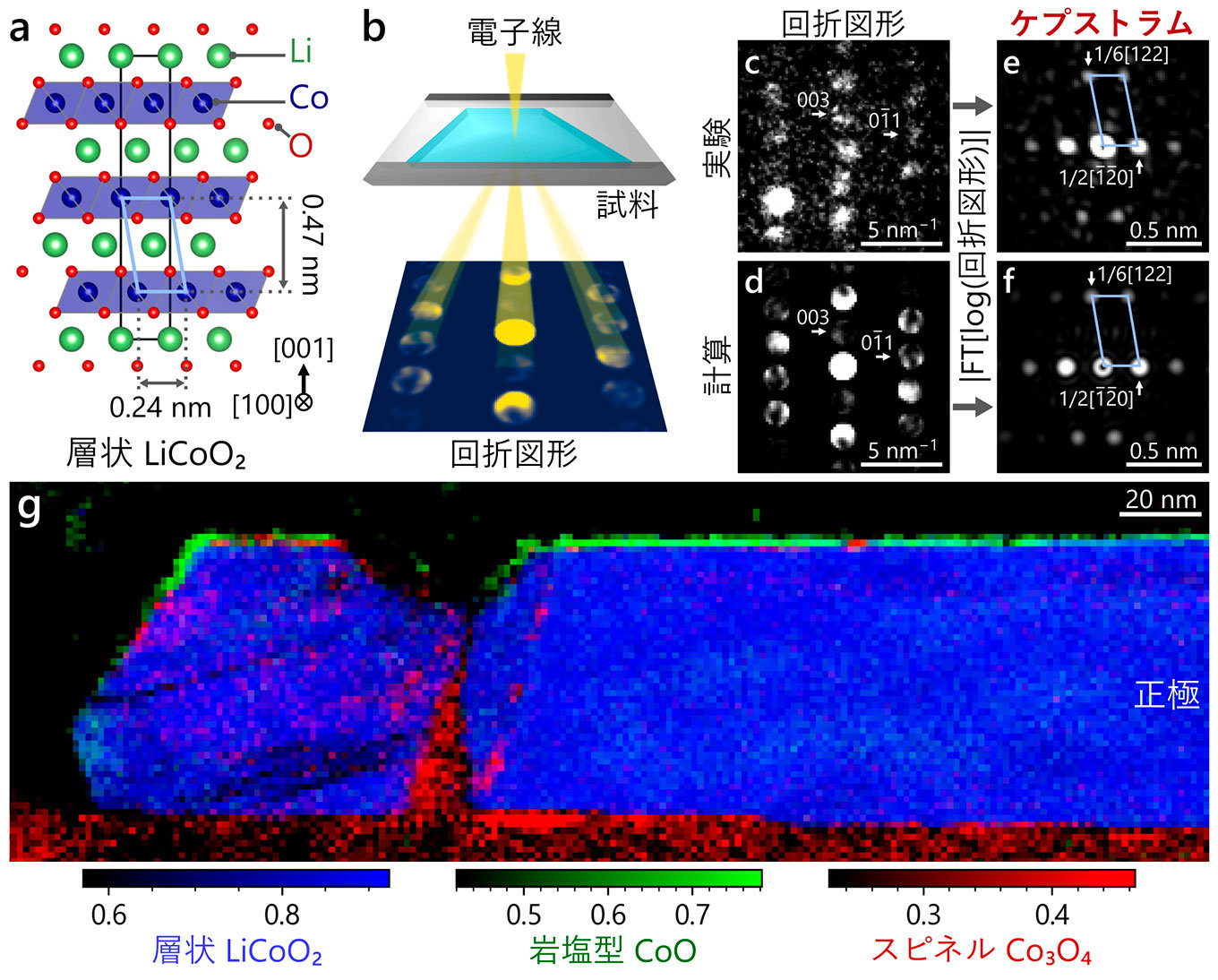
本研究グループでは、層状正極の代表例であるコバルト酸リチウム(LiCoO2)の構造(図1a)を調べるために、先進的な電子顕微鏡手法の一つである走査ナノビーム電子回折*3に注目しました (図1b)。これは、直径約1 nmの電子線をスキャンさせながら試料に照射し、結晶構造を反映する電子回折図形を得て、高速カメラに記録する手法です。高電圧で100サイクル充放電させたエピタキシャルLiCoO2について、あるスキャン位置での回折図形(図1c)と、結晶構造モデルから計算した回折図形(図1d)とで差異が認められます。電子回折図形には、結晶構造の情報に加えて、試料の厚さや僅かな傾きに依存するスポットの強度変化が含まれるため、比較が困難です。
そこで、音声信号処理で用いられるケプストラム解析*4に着目しました。ケプストラムは、回折図形の強度を対数変換してフーリエ変換し、その振幅を得ることで求められます。実験と計算のケプストラム(図1e、f)では、試料の厚さや傾きを反映する成分は中心スポットに、結晶構造の周期性を反映する成分は周囲のスポットにそれぞれ分離されます。構造由来のスポットは実験と計算でよく一致するため、この領域が層状構造だと分かります。この一致度は、相互相関関数(2つの画像が似ているほど高い値を示す関数)を用いることで、数値として評価できます。層状構造に加えて、スピネルや岩塩構造についても同様の解析を行い、試料各位置での構造を調べました。独自に開発した一連の解析を「ケプストラム照合解析」と名付けました。
結晶構造の合成マップ(図1g)では、LiCoO2正極の大部分はもとの層状構造を保持していましたが、電解質との界面から正極側へ約3 nmにかけてスピネル・岩塩構造が観察されました。本手法は、約1 nmの高空間分解能と、正極の内部と界面の両方をカバーする約300×100 nm2の広視野を同時に達成しました。さらに、原子分解能電子顕微鏡など電子線を多用する他の手法と比べ、本手法の照射量は2ケタ以上低いことが分かりました。観察中の試料損傷を低減でき、従来手法よりも信頼性の高い結果が得られます。
界面での構造変化に対して、LiCoO2正極を別の物質でコーティングして保護する対策や、異なる元素をわずかに添加する対策が提案されています。さらに、次世代デバイスとして注目を集めている全固体LIBでも、ナノスケールの構造変化が生じると報告されています。今後、本手法を活用することで、劣化メカニズムの詳細な解明や、コーティングや添加などの効果の検証を計画しています。本成果は、LIBの現象解明を目指す学術研究や、高性能LIB開発に広く貢献すると期待されます。

| 図1(a)[100]方位から見た層状LiCoO2の結晶構造モデル。(b)走査ナノビーム電子回折の模式図。(c)実験と(d)計算の電子回折図形。(e)実験と(f)計算のケプストラム。中心以外の明るいスポットが結晶構造に由来します。(g)結晶構造の合成マップ。青、緑、赤色が強いほど、層状、岩塩、スピネル構造であることを示します。 |
【研究資金】
本研究の一部は、日本学術振興会(JSPS) 科研費(JP22K14473、JP25K18108、JP24H00042)、科学技術振興機構(JST) 革新的GX技術創出事業(GteX)プログラム(JPMJGX23S5、JPMJGX23S6)、同 戦略的創造研究推進事業 先端的低炭素化技術開発(ALCA)、物質・材料研究機構(NIMS) 連携拠点推進制度、三谷研究開発財団、澁谷学術文化スポーツ財団、池谷科学技術振興財団、中部電気利用基礎研究振興財団、旭硝子財団、北陸先端科学技術大学院大学 研究拠点形成支援事業の支援を受けて実施されました。本研究の一部は、NIMS蓄電池基盤プラットフォーム、マテリアル先端リサーチインフラ(JPMXP1222JI0007、JPMXP1223JI0012、JPMXP1224JI0005)にて実施されました。
【論文情報】
| 雑誌名 | Nano Letters |
| 論文名 | Low-Dose Nanoscale Visualization of Crystal Phases in Epitaxial Cathodes via Cepstral Matching of Scanning Nanobeam Electron Diffraction |
| 著者 | Kohei Aso, Takafumi Kakeya, Takumu Tsuchida, Hiroki Ito, Sho Asano, Kenta Watanabe, Kazutaka Mitsuishi, Koji Kimoto, Keisuke Shinoda, Takuya Masuda, Masaaki Hirayama, and Yoshifumi Oshima |
| 掲載日 | 2025年10月21日 |
| DOI | 10.1021/acs.nanolett.5c03692 |
【用語説明】
目的の物質を、基板の結晶構造に合わせて成長させた薄膜。本研究ではチタン酸ストロンチウム(SrTiO3)(111)基板上に成長させたLiCoO2薄膜を用いています。結晶方位や露出表面を制御できるため、通常の粉末多結晶正極よりも観察が容易になります。
おおむね、層状LiCoO2からリチウム(Li)が抜けて、そこに一部のコバルトが入り込んだ構造。層状構造ではLiイオンが(003)面内を2次元的に移動できますが、スピネル構造や岩塩構造ではその経路が失われるため、Liイオン伝導性が低下します。さらに、一度これらの構造に変化すると層状構造には戻りにくくなります。そのため、高電圧で充放電を繰り返すとLIBの劣化につながります。特に、充電の最大電圧が4.2V(vs Li/Li+)超えたときに現れやすいです。
細く絞った電子線を試料上で走査し、各位置で電子回折図形を記録する手法。回折波の配置を解析することで、試料の結晶構造を求めることができます。実空間2次元と逆空間2次元に対する強度を示す、複雑かつ膨大な4次元データが得られるため、適切なデータ処理を施して情報を抽出する必要があります。
音声を解析するために開発された、信号の細かく変化する成分となだらかに変化する成分を分離する信号処理手法。音声分野では、声帯での原音成分と、口や鼻での共鳴によって原音から変化した成分とを分離する目的で用いられます。
令和7年10月28日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2025/10/28-2.htmlがん光免疫療法のための多機能性液体金属ナノ複合体の開発に成功! ~乳酸菌と液体金属の革新的融合により、がんの可視化・診断・治療の一体化を実現~
がん光免疫療法のための多機能性液体金属ナノ複合体の開発に成功!
~乳酸菌と液体金属の革新的融合により、がんの可視化・診断・治療の一体化を実現~
【ポイント】
- 乳酸菌成分と液体金属からなる革新的ナノ複合体の作製に世界で初めて成功
- マウス移植がんの可視化と治療効果を実証
- 免疫賦活化(活性化)と光熱変換の相乗効果により、近赤外光照射でがんを完全消失
- 優れた生体適合性を確認、新たながん診断・治療技術創出への期待
| 北陸先端科学技術大学院大学 物質化学フロンティア研究領域の都 英次郎教授らの研究チームは、液体金属*1表面に乳酸菌*2成分と近赤外蛍光色素(インドシアニングリーン*3)を被覆した多機能性ナノ複合体の開発に成功しました。 開発したナノ複合体は、EPR効果*4により、がん細胞を標的とする能力に優れており、大腸がんを移植したマウスの腫瘍内に効果的に集積することを確認しました。さらに、生体透過性の高い近赤外レーザー光*5照射により、以下の治療効果を実現しました。
実際に、近赤外光を2日に1回5分間、計2回照射することで、マウスの移植がんを5日後に完全消失させることに成功しました。また、包括的な生体適合性試験により、本ナノ複合体の高い安全性も確認されています。
本研究成果は、診断と治療を統合した革新的ながん光免疫治療技術の創出につながる可能性が期待されます。 |
【研究背景と内容】
液体金属ナノ粒子への着目
ガリウム・インジウム(Ga/In)合金からなる室温液体金属は、優れた生体適合性と物理化学的特性を有し、バイオメディカル応用において世界的に注目されています。都教授らは、「免疫賦活化物質を液体金属と組み合わせ、がん患部に選択的送達できれば、強力な抗腫瘍効果と近赤外光を用いた診断・治療の統合が実現できる」との着想から研究を開始しました(図1)。
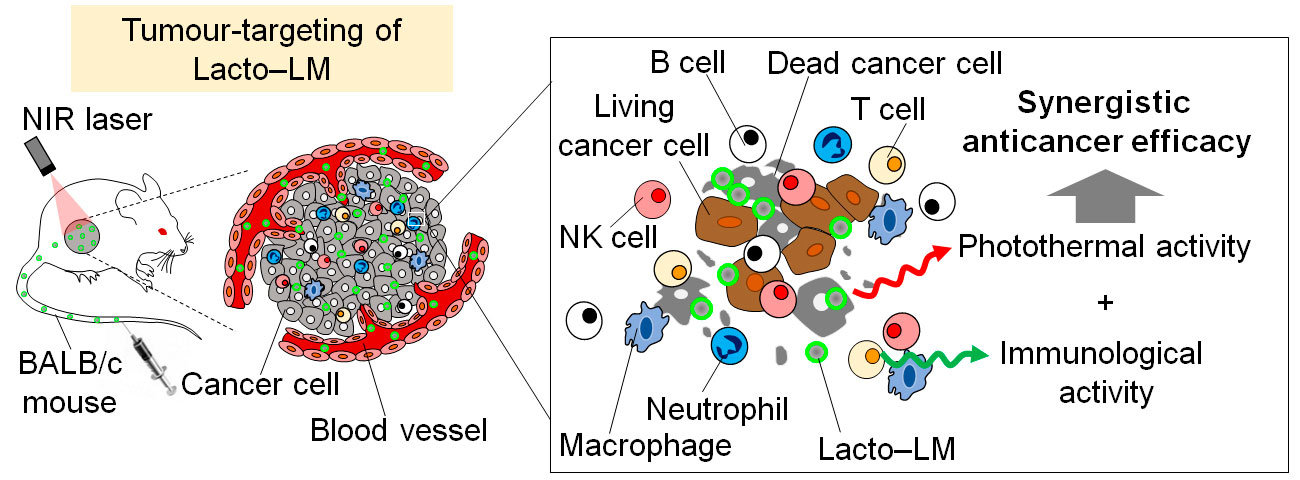
図1. 多機能性液体金属ナノ複合体を活用したがん光免疫療法の概念図
腫瘍内細菌叢の活用
近年の研究により、腫瘍組織内には固有の細菌叢(さいきんそう:細菌の集まり)が存在することが明らかになっています。都教授らは、これまでに腫瘍内から多種の細菌の単離に成功し、これらを活用したがん治療技術開発を進めてきました(既報プレスリリース:「阿吽の呼吸で癌を倒す!(※1)」「2種の細菌による新たながん治療へのアプローチ『AUN(阿吽)』を開発(※2)」)。
(※1)https://www.jaist.ac.jp/whatsnew/press/2023/05/08-1.html
(※2)https://www.jaist.ac.jp/whatsnew/press/2025/08/06-1.html
革新的ナノ複合体の創製
本研究チームは、Ga/In液体金属、乳酸菌成分、インドシアニングリーンを混合し、超音波照射するだけで球状ナノ粒子を形成する簡便な製法を確立しました。この手法により作製されたナノ複合体は以下の特性を示しました。
・高い安定性:7日以上の粒径安定性を維持
・優れた細胞親和性:高い膜浸透性と無毒性
・効率的光熱変換:近赤外光照射による発熱機能
卓越した治療効果の実証
大腸がん移植マウスを用いた評価実験では、ナノ複合体の尾静脈投与24時間後、740~790 nmの近赤外光照射により、がん患部のみが鮮明に蛍光発光し、EPR効果による選択的腫瘍集積が確認されました(図2A)。
続いて808 nmの近赤外光を患部に照射(2日間隔で各5分間、計2回)したところ、免疫賦活化と光熱変換の相乗効果により、5日後にがんの完全消失を達成しました(図2B)。
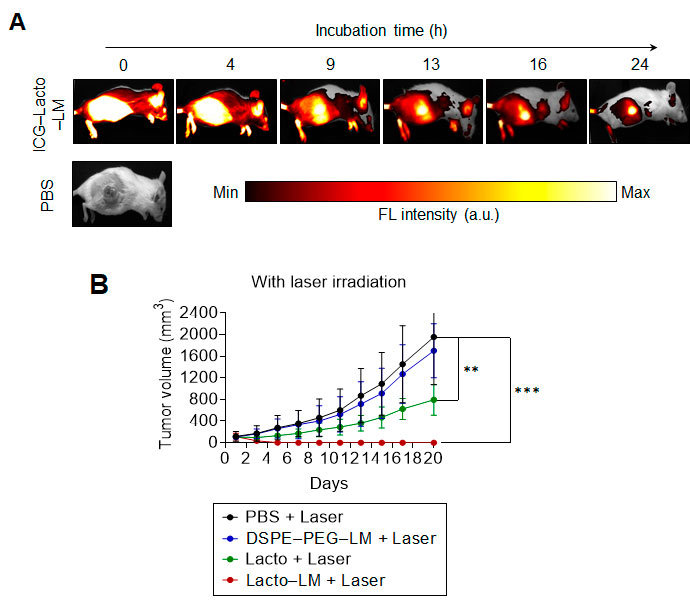
| 図2. (A) 液体金属ナノ粒子の標的腫瘍内における蛍光特性 (B) 液体金属ナノ粒子による抗腫瘍効果(腫瘍は完全消失) |
対照実験の結果
乳酸菌単独投与:免疫賦活化によりある程度の抗腫瘍効果を確認
免疫非活性化ナノ粒子(ポリエチレングリコール-リン脂質複合体*6被覆):レーザー照射後も顕著な抗腫瘍効果なし
これらの結果から、乳酸菌成分による免疫賦活化と液体金属の光熱変換の相乗効果が、強力な抗腫瘍作用をもたらすことを明確に示しています。
優れた安全性の確認
細胞毒性試験:マウス大腸がん細胞(Colon26)およびヒト正常線維芽細胞(TIG103)において、ナノ複合体投与24時間後もミトコンドリア活性を指標とした細胞生存率に低下はなく、細胞毒性がないことを確認しました。
生体適合性試験:マウス静脈内投与後の血液検査(1週間)および体重測定(約1ヵ月)において、生体への悪影響は極めて軽微であることが判明しました。
【研究の意義と今後の展望】
本研究成果は、開発したナノ複合体が次世代がん診断・免疫療法の基盤技術となり得ることを実証するものです。さらに、ナノテクノロジー、光学、免疫学の学際的融合による材料設計の新たな技術基盤として、幅広い研究領域への貢献が期待されます。
今後は、他のがん種への適用拡大や臨床応用に向けた更なる安全性・有効性検証を進め、患者さんにより優しく効果的ながん治療法の実現を目指します。
【掲載誌情報】
本成果は、材料科学系トップジャーナル「Advanced Composites and Hybrid Materials」誌(Springer Nature社発行)に9月19日(現地時間)に掲載されました。
【研究支援】
本研究は、文部科学省科研費 基盤研究(A)(23H00551)、同 挑戦的研究(開拓)(22K18440、25K21827)、国立研究開発法人 科学技術振興機構(JST)大学発新産業創出基金事業 スタートアップ・エコシステム共創プログラム(JPMJSF2318)、本学超越バイオメディカルDX研究拠点ならびに本学生体機能・感覚研究センターの支援のもと行われたものです。
【論文情報】
| 掲載誌 | Advanced Composites and Hybrid Materials |
| 論文題目 | Bacterial-adjuvant liquid metal nanocomposites for synergistic photothermal immunotherapy |
| 著者 | Nina Sang, Seigo Iwata, Yun Qi, Eijiro Miyako* |
| 掲載日 | 2025年9月19日にオンライン版に掲載 |
| DOI | /10.1007/s42114-025-01434-7 |
【用語説明】
室温以下あるいは室温付近で液体状態を示す金属のこと。例えば、水銀(融点マイナス約39℃)、ガリウム(融点約30℃)、ガリウム-インジウム合金(融点約15℃)がある。
糖から乳酸を生成する性質を有する細菌の総称。本研究で用いた乳酸菌は都研究室にて腫瘍内から単離したものである。
肝機能検査に用いられる緑色色素のこと。近赤外レーザー光を照射すると近赤外蛍光と熱を発することができる。
100nm以下のサイズに粒径が制御された微粒子は、正常組織へは漏れ出さず、腫瘍血管からのみ、がん組織に到達して患部に集積させることが可能である。これをEPR効果(Enhanced Permeation and Retention Effect)という。
レーザーとは、光を増幅して放射するレーザー装置、またはその光のことである。レーザー光は指向性や収束性に優れており、発生する光の波長を一定に保つことができる。とくに700~1100 nmの近赤外領域の波長の光は生体透過性が高いことが知られている。
ポリエチレングリコールとリンを含有する脂質(脂肪)が結合した化学物質。脂溶性の薬剤を可溶化させる効果があり、ドラッグデリバリーシステムに良く利用される化合物の一つ。
令和7年9月25日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2025/09/25-1.html物質化学フロンティア研究領域の都教授らの総説論文がCell Biomaterialsに掲載
物質化学フロンティア研究領域の都 英次郎教授らの総説論文「生きた医薬(リビングドラッグ):治療応用における素晴らしい進化(Living Drugs: A Wonderful Evolution for Therapeutic Applications)」が、国際学術誌 Cell Biomaterials(Nature姉妹誌と同等レベルに格付けされているCell Pressの新興フラッグシップジャーナル)に掲載されました。
なお、本研究は、文部科学省 科学研究費補助金 基盤研究A(23H00551)、同 挑戦的研究(開拓)(22K18440、25K21827)、国立研究開発法人 科学技術振興機構(JST)研究成果最適展開支援プログラム(A-STEP)(JPMJTR22U1)、同 大学発新産業創出基金事業 スタートアップ・エコシステム共創プログラム(JPMJSF2318)、同 次世代研究者挑戦的研究プログラム(SPRING)未来創造イノベーション研究者支援プログラム(JPMJSP2102)、本学超越バイオメディカルDX研究拠点ならびに生体機能・感覚研究センターの支援のもと行われたものです。
掲載誌 :Cell Biomaterials
論文題目:Living Drugs: A Wonderful Evolution for Therapeutic Applications
著者 :Soudamini Chintalapati, Nina Sang, Mikako Miyahara, Seigo Iwata, Kei Nishida, Eijiro Miyako*
掲載日 :2025年9月8日にオンライン版に掲載
DOI :https://doi.org/10.1016/j.celbio.2025.100193
■論文概要
本総説では、細菌・ウイルス・ファージなどの「生きた医薬(Living Drugs)」が持つ治療応用の最前線と将来展望について包括的に解説しています。特に、がんや多剤耐性菌感染症において、これらの生物を利用した革新的治療法が急速に進展しており、免疫応答の回避、標的精度の向上、複合療法モデルの構築など、多様な技術的ブレークスルーが紹介されています。さらに、臨床応用に向けた課題として、投与方法や安全性評価、規制面での対応などが議論され、治療カテゴリーごとの将来方向性や研究優先課題についても提案しています。
本総説では、都研究室が開発を進めている2種の細菌による新たながん治療へのアプローチ「AUN(阿吽)」(プレスリリース参照)を用いた新規がん療法についても取り上げています。AUNは低酸素性腫瘍微小環境に選択的に集積・増殖し、免疫依存性と免疫非依存性の両経路を介して腫瘍を攻撃する自然由来の細菌療法です。特に、免疫不全状態でも効果を発揮し、腫瘍内血管の選択的破壊や細菌変形などによる直接的な腫瘍壊死誘導が確認されています。遺伝子改変を必要とせず高い安全性を維持できることから、臨床応用への展望が広がっています。
本総説は、Living Drugs研究の現状と課題、そして都研究室発のAUN療法を含む次世代治療の可能性を示す重要な指針となるものです。
プレスリリース詳細:2種の細菌による新たながん治療へのアプローチ「AUN(阿吽)」を開発 ―免疫不全状態でも機能が期待されるがん治療に向けて―
令和7年9月9日
出典:JAIST お知らせ https://www.jaist.ac.jp/whatsnew/info/2025/09/09-1.html人と安全に協働できる"ソフトロボットリンク"を開発 触れてわかる、近づいて感じる-近接覚と触覚のハイブリッドセンシング技術「ProTac」
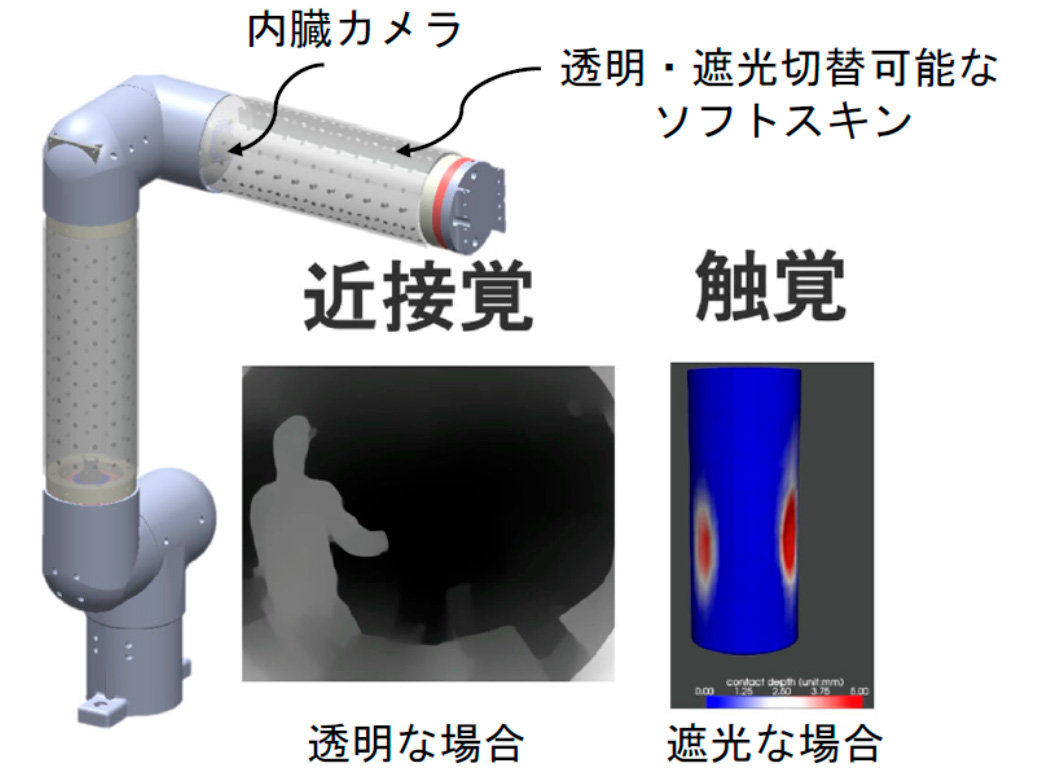
人と安全に協働できる"ソフトロボットリンク"を開発
触れてわかる、近づいて感じる-近接覚と触覚のハイブリッドセンシング技術「ProTac」
【ポイント】
- 透明・不透明を切り替えられるソフトスキンと視覚センサーを用い、近接センシングとスキン変形の解析による触覚センシングを備えたマルチモーダルソフトセンシング技術「ProTac」を開発
- 市販ロボットアームにも取り付け可能
- 従来の剛体リンクでは困難とされる、接触の多い環境下での動作制御が可能
- 農業や介護など、人とロボットが協働する作業への応用に期待
- AI駆動型センシングフュージョン技術
| 北陸先端科学技術大学院大学 ナノマテリアル・デバイス研究領域のクアン・ハン・ルウ研究員、ホ・アン・ヴァン教授らの研究チームは、透明・不透明を電圧により切り替えられるソフト素材と視覚センシング技術を融合し、近接・触覚の両モードを切り替えて検知できるマルチモーダルソフトセンシング技術「ProTac」を世界で初めて開発しました。ProTacを用いたソフトロボットリンクは、周囲の物体を検知する近接センシングとマーカー画像の変化から触覚情報を読み取る触覚センシングを一台で切り替えて行うことができ、人との接触が多い環境で安全に動作制御が可能です。なお、本研究成果は、2025年7月28日にIEEE Transactions on Robotics(T-RO)に掲載されました。 |
【研究概要】
近年、人と同じ空間で安全かつ柔軟に作業できるロボットのニーズが高まっています。これに応えるため、私たちの研究チームは、ソフト機能材料と画像や映像から情報を取得・解析する技術である視覚センシング技術を融合した新しいマルチモーダルソフトセンシング技術「ProTac」(図1)を開発しました。
ProTacは、電圧をかけることで透明・不透明を切り替えられるポリマーディスパースド液晶(PDLC)フィルム注1)と内蔵カメラを組み合わせています。透明時には視界を活用して周囲の物体の近接を検知し、不透明時にはマーカー画像の変化から触覚情報の取得を実現します。また、最新の深層学習ベースの視覚アルゴリズムを用いることで、安定したリアルタイムセンシングが可能です。

図1:ProTacのイメージ図
この技術を用いたソフトロボットリンクは、市販のロボットアームやカスタム製作されたソフトロボットにも取り付け可能で、障害物検知に基づく速度調整や接触時の反射動作など、多様な制御戦略を実現します。ProTacを備えたソフト多機能センシングアームは、人とロボットが密に連携する場面や、従来の剛体リンクでは困難な動作制御において高い性能を示しました。
今後は、この技術を手足や胴体などロボットの各部位に応用し、高機能なマルチモーダルスキンを備えたヒューマノイドロボットの実現が期待されます。また、農業、家庭サービス、介護分野など、幅広い分野での応用も見込まれます。
【研究資金】
本研究は、日本学術振興会 科学研究費補助金 特別研究員奨励費(24KJ1203)、国立研究開発法人 科学技術振興機構(JST)さきがけ(JPMJPR2038)による財政的支援を受けて実施されました。
【論文情報】
| 掲載誌 | IEEE Transactions on Robotics |
| 論文タイトル | Vision-based Proximity and Tactile Sensing for Robot Arms: Design, Perception, and Control |
| 著者 | Quan Khanh Luu, Dinh Quang Nguyen, Nhan Huu Nguyen, Nam Phuong Dam, Van Anh Ho |
| 掲載日 | 2025年7月28日 |
| DOI | 10.1109/TRO.2025.3593087 |
【用語説明】
電圧により透明・不透明を切り替えられる液晶材料。柔軟であり、ディスプレイやスマートウィンドウなどの光の透過を制御する用途に使用される。
令和7年8月22日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2025/08/22-1.html物質化学フロンティア研究領域の都教授らの論文がSpringer Nature Research CommunitiesのBehind the Paperで紹介
物質化学フロンティア研究領域の都 英次郎教授らの最新の論文「2種の細菌による新たながん治療へのアプローチ『AUN(阿吽)』を開発―免疫不全状態でも機能が期待されるがん治療に向けて―」が、Springer Nature Research CommunitiesのBehind the Paperにて紹介されました。研究開発の発端、裏話などが紹介されています。なお、本研究は、文部科学省 科学研究費補助金 基盤研究A(23H00551)、同 挑戦的研究(開拓)(22K18440、25K21827)、国立研究開発法人 科学技術振興機構(JST) 研究成果最適展開支援プログラム(A-STEP)(JPMJTR22U1)、同 大学発新産業創出基金事業 スタートアップ・エコシステム共創プログラム(JPMJSF2318)、同 次世代研究者挑戦的研究プログラム(SPRING) 未来創造イノベーション研究者支援プログラム(JPMJSP2102)、公益財団法人 発酵研究所、公益財団法人 上原記念生命科学財団、本学超越バイオメディカルDX研究拠点、本学生体機能・感覚研究センターならびに第一三共株式会社の支援のもと行われたものです。
■論文概要
本研究では、2種類の細菌がまるで"阿吽の呼吸"のように精緻に連携しながら、がん細胞を選択的に攻撃するという新たな治療へのアプローチ「AUN(阿吽)」の開発に成功しました。
研究チームが用いたのは、"AUN(阿吽)"と名付けられた2種の天然細菌:腫瘍内に常在するProteus mirabilis[阿形(A-gyo)]と、光合成を行うRhodopseudomonas palustris[吽形(UN-gyo)]です。この互いに異なる機能を持つ2種の細菌が、それぞれの役割を果たしながら、以下の一連のプロセスを協調的に引き起こし、抗腫瘍効果を示すことが確認されました。まず、がん特有の環境に誘導されて、両細菌はマウス皮下腫瘍モデルにおいて腫瘍の血管やがん細胞を選択的に破壊。これにより、正常組織への影響を最小限に抑えつつ、がん組織だけを効果的に抑制する可能性が示唆されました。さらに、がんが産生する特異的な代謝物の存在下で、片方の細菌(A-gyo)は線維状の構造へと変化。この形態変化により抗腫瘍効果が一段と強化されることが判明しました。興味深いのは、経時的に両細菌の集団構成(ポピュレーション)も動的に変化し、最適な役割分担が自然に形成される点です。加えて、病原性を抑制しながら、重篤な副作用の原因となるサイトカインストームの発生も回避できる可能性があるという点も特徴です。
本研究は、2種の細菌の持つ自然な"協調戦略"を巧みに活用することで、安全かつ効果的ながん治療の新たな道を拓くものです。今後、このメカニズムを応用した新しいがん治療法の社会実装に向けて、スタートアップ創業を計画しています。
プレスリリース詳細:2種の細菌による新たながん治療へのアプローチ「AUN(阿吽)」を開発 ―免疫不全状態でも機能が期待されるがん治療に向けて―
令和7年8月7日
出典:JAIST お知らせ https://www.jaist.ac.jp/whatsnew/info/2025/08/07-2.html糖鎖による抗体ダイナミクスの制御機構を解明 ~分子経絡が抗体医薬設計の新たな鍵に~
  |
| 大学共同利用機関法人 国立大学法人 東京科学大学 公立大学法人 名古屋市立大学 ⼀般財団法人 国立大学法人 大阪大学 国立大学法人 |
糖鎖による抗体ダイナミクスの制御機構を解明
~分子経絡が抗体医薬設計の新たな鍵に~
自然科学研究機構(生命創成探究センター)の谷中冴子 准教授(現 東京科学大学 准教授)、加藤晃⼀ 教授(生命創成探究センター、名古屋市立大学)らは、抗体の糖鎖修飾、特にガラクトース付加が、抗体分子の構造と動態に及ぼす影響を原子レベルで解明しました。
本研究の成果は、国際科学雑誌 「Proceedings of the National Academy of Sciences of the United States of America(米国科学アカデミー紀要)」に掲載予定です。論文は日本時間2025年8月5日の週にオンライン公開される予定であり、DOIおよび掲載URLは公開後に付与されます。
【発表のポイント】
私たちの体には、病原体から身を守るための免疫システムが備わっています。その中心的な役割を担うのが「免疫グロブリンG(IgG)」注1) と呼ばれる抗体です。IgGは、特定の抗原を認識して結合するだけでなく、Fc受容体や補体といったエフェクター分子との相互作用を通じて、様々な免疫応答を誘導します。本研究では、IgGのFc領域 注2) に結合した「糖鎖」の修飾が、IgGの動的な構造変化を制御し、その結果として免疫機能が調節されるメカニズムを、計算科学と実験科学を融合したアプローチで明らかにしました。特に、本研究では、糖鎖修飾による影響が、あたかも私達の体の中に張り巡らされた経絡のように、分子レベルで伝播していく「分子経絡」注3) の重要性に着目しました。
【研究の背景】
治療用抗体は、がんや自⼰免疫疾患など、さまざまな疾患の治療に用いられています。抗体の効果は、標的抗原への結合だけでなく、Fc領域を介したエフェクター機能 注4) の発揮によっても大きく左右されます。Fc領域の糖鎖修飾 注5) は、抗体のエフェクター機能を調節する重要な因子であり、そのメカニズム解明は、より効果的な抗体医薬品の開発につながると考えられています。
【本研究の手法と成果】
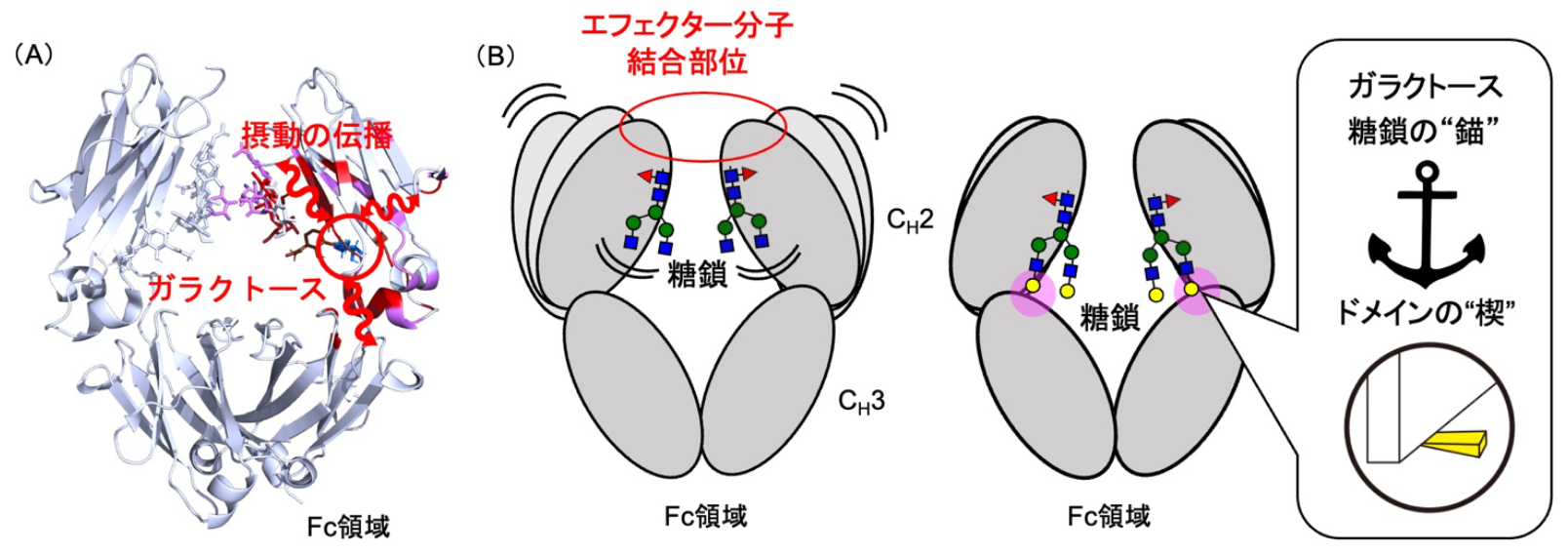
研究グループは、遺伝子工学的手法と酵素反応を組み合わせることで、糖鎖構造が異なるIgG1-Fcを調製しました。これらについて、安定同位体標識NMR分光法 注6) を用いてFc領域の動的構造を解析するとともに、分子動力学シミュレーション 注7) によって糖鎖修飾がFc領域のコンフォメーション変化に与える影響を評価しました。また、動的ネットワーク解析を用いて、「分子経絡」を同定しました。NMR分光法と分子動力学シミュレーションの結果から、ガラクトース 注8) 残基は糖鎖の動きを止める「錨」およびFc領域全体の動きを抑える「楔」としてはたらき、フコース 注9) 除去は特定のFc受容体との結合に関与するアミノ酸残基の動態を変化させることが明らかになりました。これらの結果は、糖鎖修飾がIgGのFc領域の動的構造を制御し、エフェクター機能を調節するメカニズムを原子レベルで理解する上で重要な知見となります。特に、「分子経絡」の存在は、糖鎖修飾の効果がFc領域全体に伝播する様子を示唆しています。

| (図)(A)糖鎖のガラクトース残基での構造変化がFc分子内を伝わる様子を示している。(B)ガラクトース残基は糖鎖(黄色の丸)の動きを止める「錨」およびFc領域全体の動きを抑える「楔」としてはたらき、エフェクター分子との相互作用を助けている。 |
【成果の意義および今後の展開】
本研究成果は、治療用抗体の開発において、Fc領域の糖鎖修飾を最適化するための合理的な設計基盤を提供します。今後は、糖鎖修飾と抗体の構造・機能相関に関するさらなる研究を進めることで、また「分子経絡」の操作という新たな視点を取り入れることで、より効果的かつ安全な抗体医薬品の開発に貢献できると期待されます。
【用語解説】
【論文情報】
| 掲載誌 | Proceedings of the National Academy of Sciences of the United States of America |
| タイトル | Exploring Glycoform-Dependent Dynamic Modulations in Human Immunoglobulin G via Computational and Experimental Approaches |
| 著者 | Saeko Yanaka, Yoshitake Sakae, Yohei Miyanoiri, Takumi Yamaguchi, Yukiko Isono, Sachiko Kondo, Miyuki Iwasaki, Masayoshi Onitsuka, Hirokazu Yagi, Koichi Kato*(*責任著者) |
| DOI | |
| 掲載日 |
【著者情報】
東京科学大学 総合研究院 フロンティア材料研究所)
名古屋市立大学大学院薬学研究科)
【研究サポート】
本研究は、文部科学省科学研究費助成事業(JP20K15981 および JP23K24018 谷中冴子、JP19H01017 および JP24H00599 加藤晃⼀)、日本医療研究開発機構(AMED)(JP21ae0121020 および JP23ak0101209 谷中冴子、JP21ae0121013 加藤晃⼀)、文部科学省研究大学総合研究育成事業:研 究大学強化促進事業(CURE)課題番号JPMXP1323015488(Spin-LプログラムNo. spin24XN014)、生命創成探究センター共同利用研究(24EXC901、25EXC603)、および科学技術振興機構(JST)戦略的 創造研究推進事業(CREST)(JPMJCR21E3 加藤晃⼀)の助成を受けたものです。また、本研究は文部 科学省ナノテクノロジープラットフォーム事業(分子・物質合成)、大阪大学蛋白質研究所共同利用・共 同研究拠点 NMRCR-16-05, 17-05, 18-05, 19-05, 20-05, 21-05、計算科学研究センター(24-IMS-C197)、文部科学省先端研究設備共用促進事業(コアファシリティ構築支援プログラム)JPMXS0441500024、国際・産学連携インヴァースイノベーション材料創出(DEJI2MA)プロジェクト、およびヒューマングライコームプロジェクトの支援を受けて行われました。
令和7年8月5日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2025/08/05-1.html次世代プロトン電池へ期待 ―多孔質MXene(マキシン)フィルムが高容量・高速充電を実現―
次世代プロトン電池へ期待
―多孔質MXene(マキシン)フィルムが高容量・高速充電を実現―
ポイント
- 次世代電池「プロトン電池」の鍵となる多孔質MXene (マキシン)フィルムを開発
- 素材の穴の量(細孔密度)を調整することで、従来を大きく上回る電池容量と充電性能を実現
- 長寿命でエコな電池づくりに前進、持続可能なエネルギー社会に貢献
| 北陸先端科学技術大学院大学 物質化学フロンティア研究領域のLinh Chi T. Cao大学院生(博士後期課程)、青木健太郎助教、長尾祐樹教授らは、タイ・タマサート大学シリントン国際工学部(SIIT)およびタイ・国立電子コンピューター技術研究センター (NECTEC)と共同で、再生可能エネルギーの普及や電気自動車の進化に伴い需要が高まる高性能エネルギー貯蔵デバイスの実現に向け、次世代型プロトン電池*1の鍵となる多孔質MXene*2,3アノード(陽極)の開発に成功しました。 本研究で開発された多孔質MXeneフィルムは、MXeneを用いた先行研究の中で最高の性能を発揮し、高容量と超高速充電を両立できることが示されました。この成果は、環境負荷の低い、持続可能な電池技術の発展に大きく貢献すると期待されます。 |
【背景】
現代社会では、電気自動車の普及や携帯端末の進化に伴い、効率の良いエネルギー貯蔵システムの重要性が高まっています。長く市場を牽引してきたリチウムイオン電池は、リチウム資源の限界、環境への影響、安全性といった課題を抱えており、資源の乏しい日本が持続可能な発展を遂げるためには、多様なエネルギー資源の活用と高効率な変換技術の確立が不可欠です。
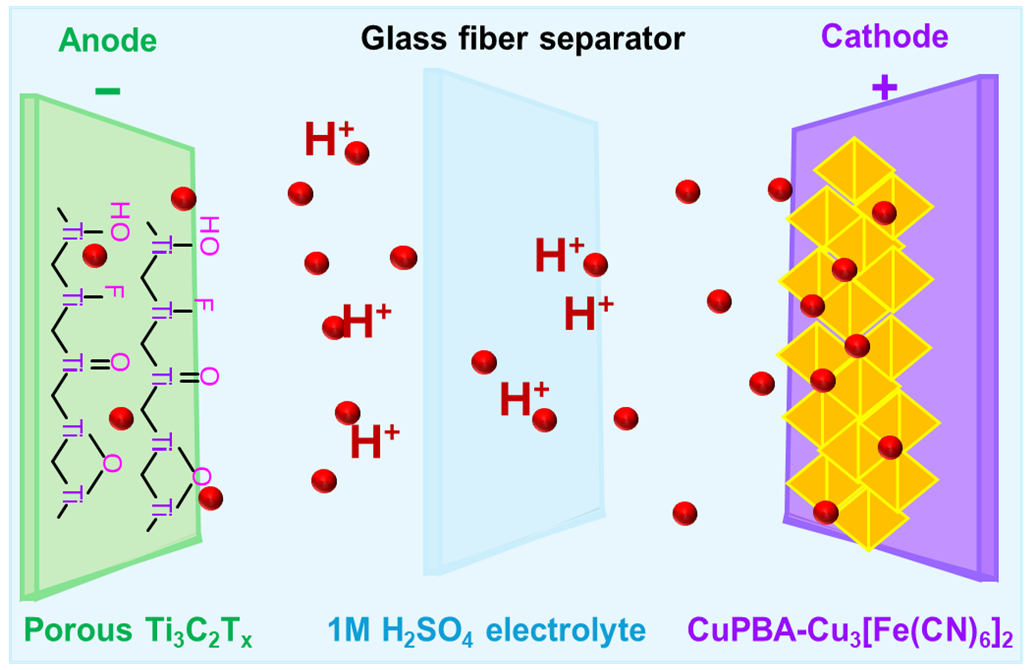
そこで注目されているのが、プロトンと呼ばれる水素原子(H+)を電荷キャリアとして利用するプロトン電池(図1)です。プロトン電池は、水素イオンを使って電気をやりとりする電池で、材料が豊富でエコ、かつ素早く充電できる可能性を秘めており、次世代エネルギー貯蔵の有力候補として注目されています。二次元のナノ材料であるMXeneは、その優れた電気伝導性や高い表面積から、プロトン電池の有望なアノード候補です。しかし、従来のMXeneを薄膜状にしたMXeneフィルムは、MXeneのシート間の相互作用が強く、反応が起こる場所が減少したり、プロトンの輸送が阻害されたりといった課題を抱え、その性能を十分に引き出せていませんでした。

図1 本研究のプロトン電池の模式図
【成果】
本研究では、MXeneアノードの性能向上を目指し、ある物質を鋳型(テンプレート)として利用してその鋳型を犠牲にすることで目的とする物質構造を形成する合成手法である「犠牲テンプレート法」を用いて、細孔密度を系統的に調整した多孔質MXene(P-MX)フィルムを開発しました(図2)。特に、ポリ乳酸(PLA)とMXeneの比率が1:8の条件で合成された「1:8P-MX」アノードは、1 A g−1で104.8 mAh g−1という高容量を達成し、2000サイクル後も96.7%の容量維持率を維持しました(図3)。これは、これまでに報告されたMXeneアノードの中で最高の性能です(図4)。これは、電池を繰り返し使う中で、電解液が素材のすき間にしみ込みやすくなり、さらにプロトンが出入りすることで、素材同士がくっついてしまうのを防ぎ、性能の低下を抑えることができ、反応が起こる場所の増加に繋がったためと考えられます。
さらに、1:8P-MXアノードと銅鉄プルシアンブルー類似体*4(CuPBA)カソード(陰極)を組み合わせた「フルセル」プロトン電池を構築しました。この「フルセル」は、1 mol L−1 H2SO4電解液中で、1 A g−1(17 C)で57.9 mAh g−1、そして10 A g−1(188 C)という高速充電レート*5においても53.3 mAh g−1という高い容量を保持しました。二次電池(充電可能な電池)の充放電におけるエネルギー効率を表す指標である「クーロン効率」は200サイクル後も97%と安定して高い値を示しましたが、容量維持率は65.4%に低下しました。これは、主にCuPBAカソードの電解液中での溶解・分解に起因すると特定され、今後の課題となります。これらの結果は、MXeneアノードにおける細孔設計が、容量とレート性能の両方を向上させる上で極めて重要であることを示しています。

図2 多孔質MXene(P-MX)フィルムの走査電子顕微鏡観察
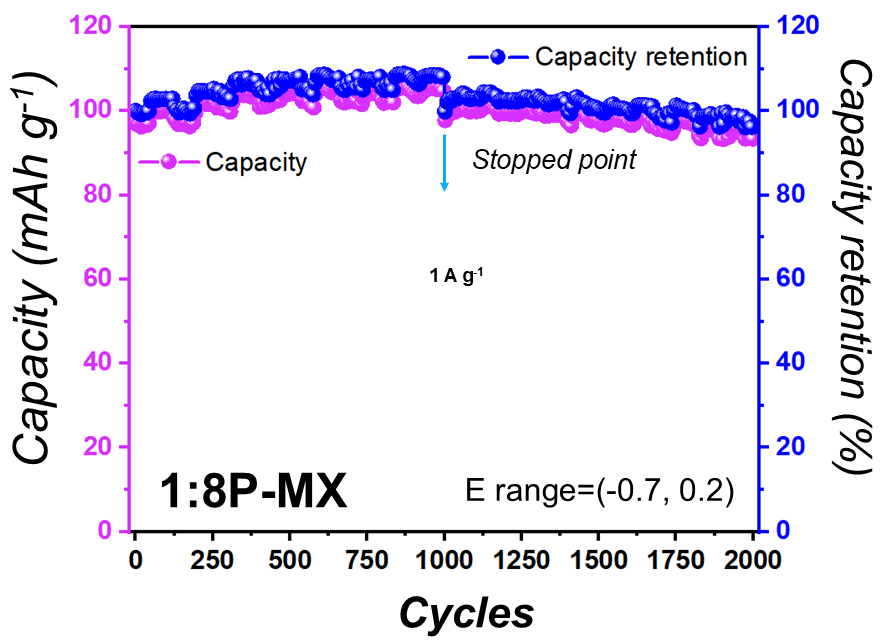
図3 1:8P-MXフィルムのサイクル特性:電流密度1 A g-1、
電位範囲 −0.7~0.2 Vにおける容量(左軸)および容量保持率(右軸)
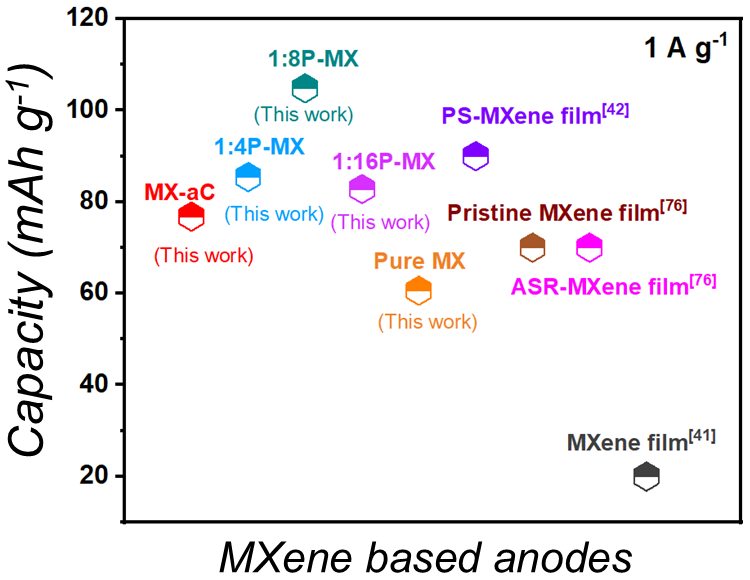
図4 本研究におけるMXeneベースのアノード性能と文献との比較
【社会への還元として期待できる内容、今後の展望】
本研究の成果は、最適化された細孔設計を持つMXeneアノードが、高容量で高速充電が可能な次世代プロトン電池の実現に大きく貢献することを示しています。特に、高濃度酸性電解液や追加の活性材料を用いずに、MXeneのみで高性能を実現した点は、環境への影響を低減し、より持続可能なエネルギー貯蔵システムを開発する上で重要な進歩です。今後は、フルセル電池の長期安定性をさらに向上させるため、CuPBAカソードの電解液中での安定性改善に焦点を当てた研究を進めていきます。これにより、1:8P-MXアノードの優れた性能を最大限に引き出し、プロトン電池の実用化を目指します。
本研究は、国立研究開発法人科学技術振興機構(JST)戦略的創造研究推進事業CREST(グラント番号 JPMJCR21B3)による財政的支援を受けて実施されました。
【論文情報】
| 掲載誌 | Chemical Engineering Journal |
| 論文タイトル | Porosity-controlled MXene anodes for enhanced rate and long cycle life performance in aqueous proton batteries |
| 著者 | Linh Chi T. Cao*, Kentaro Aoki, Shu-Han Hsu, Sakoolkan Boonruang, Yuki Nagao*(筆頭著者も責任著者) |
| 掲載日 | 2025年7月15日 |
| DOI | 10.1016/j.cej.2025.165882 |
【用語説明】
プロトン(水素イオン、H+)を電荷キャリアとして利用する二次電池の一種です。資源の豊富さや高速な電荷移動が特徴です。
二次元遷移金属炭化物の一種で、高い電気伝導性と表面積を持つ有望な新素材です。
微細な穴(細孔)を多数導入したMXene材料で、電解液の浸透性やイオン輸送経路を改善し、電池性能を向上させます。
プロトン電池のカソード材料として研究される化合物群です。
電池の充電および放電速度を示す指標です。1Cは定格容量を1時間で充放電する速度を意味します。
令和7年7月17日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2025/07/17-1.html令和7年度TeSH GAPファンドプログラム『ステップ1』に本学から5名が採択されました
令和7年度TeSH GAPファンドプログラム『ステップ1』の採択者が決定し、本学からは以下5件の研究開発課題が採択されました。
| テック分野 | |
| 人間情報学研究領域 鵜木 祐史 教授 |
音声なりすまし対策のための深層情報ハイディング法/検出法の開発 |
| 物質化学フロンティア研究領域 西村 俊 准教授 |
小規模で効率的な反応評価システムが担う触媒インフォマティクスの事業展開 |
| 物質化学フロンティア研究領域 上田 純平 准教授 |
傷も付かない半永久高輝度透明蓄光セラで究極の低環境負荷光材料を実現! |
| 環境分野 | |
| バイオ機能医工学研究領域 廣瀬 大亮 講師 |
酸化物薄膜トランジスタ型センサとAIの融合技術による"誰でもできる"食品のかんたんスマート品質チェックシステムの提供 |
| 加藤 裕介 博士後期課程学生 | 革新的凍結保存技術による豚精液の凍結保存事業 |
(参考)TeSH HP>R7年度 TeSH GAPファンドプログラム『ステップ1』採択者
TeSHは、2024年2月にJSTの"大学発新産業創出基金事業(2023-2027)スタートアップ・エコシステム共創プログラム"の"地域プラットフォーム"の一つに選ばれました。TeSHが支援するGAPファンドは、基礎研究の成果をビジネスとしての可能性を評価できる段階まで引き上げる「ステップ1」と、概念実証からスタートアップ組成までを支援する「ステップ2」からなります。
令和7年5月27日
出典:JAIST お知らせ https://www.jaist.ac.jp/whatsnew/info/2025/05/27-1.html光強度と反応温度を制御するだけで、光触媒反応の律速過程を判別可能な新手法を開発

光強度と反応温度を制御するだけで、
光触媒反応の律速過程を判別可能な新手法を開発
【ポイント】
- プロセス分離の難しい光触媒反応において、「励起キャリアの表面への供給」か「表面での酸化還元反応」のどちらが律速となっているかを簡便に判別できる手法を確立
- 光照射強度と反応温度を系統的に変化させることで、光触媒表面に過剰な励起キャリアが存在し始める"しきい値"を捉え、律速段階を見極めることに成功
- ナノ粒子化や結晶性向上など、今後の光触媒材料設計における具体的な指針を提示
| 北陸先端科学技術大学院大学(学長・寺野稔、石川県能美市)物質化学フロンティア研究領域の張葉平特任助教(日本学術振興会特別研究員-PD)、谷池俊明教授らの研究グループは、光触媒反応における反応速度を決定づける律速プロセスを、光強度と反応温度を制御するだけで簡便に特定する方法を開発しました。光触媒反応は光の吸収から励起キャリアの拡散、そして表面での酸化還元反応まで複数のステップを経るため、どの段階が律速しているのかを従来は見極めにくいという課題がありました。本研究では、表面での励起キャリアが不足または余剰となる状態を温度変化から読み解く新たな指標を導入し、これにより「励起キャリアの表面への供給」と「表面での酸化還元反応」のどちらが支配的かを判別できることを示しました。今回の成果は、光触媒の性能向上や仮説検証の精度向上に加え、高効率な太陽光利用技術の開発にも波及効果が期待されます。 |
【研究の背景】
光触媒は、太陽光を活用し、水の分解による水素生成や二酸化炭素の還元、環境浄化など、多岐にわたる反応系への応用が期待されており、持続可能な社会の実現に向けた重要な技術として注目されています。しかし、光の吸収、励起キャリア(電子や正孔)の生成・拡散・表面での酸化還元反応といった複数のプロセスが絡み合うため、どの段階が律速しているかを明確にするのは容易ではなく、結果として効率的な材料改良が進みにくいという課題がありました。
【研究の詳細】
本研究では、光触媒反応を「励起キャリアの表面への供給」と「表面における酸化還元反応」の2つの過程に分け、どちらが律速となっているかを見極めるための簡便な手法を提案しました。具体的には、両過程の速度差は、表面における励起キャリアの過不足として現れ、それが光強度と反応温度を変化させた際の温度依存性として抽出されます(図1)。この考え方は、表面反応の方が温度変化に敏感であるという既知の性質を活用したもので、ある光強度以上になると温度によって反応速度が変化し始める「しきい値(オンセット強度)」が重要な指標となります。この指標を用いることで、律速過程を明確に記述できると考えました。

| 図1 光強度と反応温度の制御によって律速過程を特定する手法の概念図。反応速度に温度依存性が現れる光強度条件は、表面での励起キャリアの再結合が反応に転じる転換点に対応しており、励起キャリアの供給速度が表面反応速度を上回り始める"オンセット強度"として機能します。 |
この考えの実証に際して、代表的な光触媒である酸化チタン(TiO2)と酸化亜鉛(ZnO)を用い、メチレンブルーの分解反応をモデル反応として検証しました。反応温度を10˚Cと40 ˚Cに設定し、光強度を広範囲で制御しながら反応速度を測定した結果、TiO2では高い光強度で温度依存性が現れ、ZnOではより低い光強度から温度依存性が認められました。この結果から、相対的にTiO2はキャリア供給が律速し、ZnOは表面反応が律速すると判定され、材料ごとの律速特性の違いを明確に捉えることができました。このような判別は、材料選定や改良方針の誤りを防ぐ手がかりとなります。
さらに、酸化チタンの焼成温度を変化させた材料シリーズで同様の検討をしたところ、類似した材料においてはオンセット強度に顕著な違いが見られなかったものの、オンセット強度を超える強い光強度条件において性能と温度依存性を比較した結果、ナノサイズ化に伴ってキャリア供給が向上し、温度依存性も大きくなる傾向が確認されました。逆に、高温焼成によって粒子が大きくなった試料ではキャリア供給効率が低下し、温度変化に対する反応の応答も鈍くなりました。このことから、単なる結晶性の向上よりも、ナノ粒子化による表面へのアクセス性の向上がキャリア供給において重要であることが示唆されました。
従来のキャリア供給・移動・反応の解析には、レーザーを用いた瞬時分光法などの特殊装置や複雑な条件設定が必要でしたが、本研究で提案した手法は、一般的な光源と温度制御だけで実施可能であり、日常的な材料スクリーニングにも応用しやすい点が大きな特徴です。また、光強度の設定範囲が実使用条件に近いため、実際の性能と乖離の少ない律速過程の判定を行うことが可能です。
【今後の展望】
本手法は、光触媒の性能向上を目指した材料開発において、律速段階を簡便に特定できる有用な手段と考えられます。今後は、他の反応系や材料系への適用範囲を広げるとともに、ハイスループット実験への展開を通じて、より効率的かつ再現性のある材料評価を可能にしたいと考えています。特に、キャリア供給が律速か、あるいは表面反応が律速かを判断することは、材料改良の方向性を明確にする際に効果を発揮し、多くの光触媒研究の仮説検証に貢献できると期待されます。
【研究資金】
本研究は、日本学術振興会科研費 特別研究員奨励費(24KJ1201)、科学技術振興機構(JST) 次世代研究者挑戦的研究プログラム(JPMJSP2102)、リバネス研究費京セラ賞の支援を受けて実施されました。
【論文情報】
| 雑誌名 | Journal of Materials Chemistry A |
| 論文名 | Identifying Rate-Limiting Steps in Photocatalysis: A Temperature- and Light Intensity-Dependent Diagnostic of Charge Supply vs. Charge Transfer |
| 著者 | Yohei Cho, Kyo Yanagiyama, Poulami Mukherjee, Panitha Phulkerd, Krishnamoorthy Sathiyan, Emi Sawade, Toru Wada, and Toshiaki Taniike |
| 掲載日 | 2025年5月2日 |
| DOI | 10.1039/D5TA00415B |
令和7年5月12日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2025/05/12-1.html物質化学フロンティア研究領域の都教授らの論文がSmall Science誌の表紙に採択
物質化学フロンティア研究領域の都 英次郎教授らの「磁石と光で機能制御可能なナノ粒子の開発に成功!-高性能がん診断・治療に向けて-」に係る論文が、生物・化学系のトップジャーナルSmall Science誌の表紙に採択されました。本研究は、文部科学省科研費 基盤研究(A)(23H00551)、文部科学省科研費 挑戦的研究(開拓)(22K18440)、国立研究開発法人科学技術振興機構(JST) 研究成果最適展開支援プログラム (A-STEP)(JPMJTR22U1)、大学発新産業創出基金事業スタートアップ・エコシステム共創プログラム(JPMJSF2318)ならびに本学超越バイオメディカルDX研究拠点、本学生体機能・感覚研究センターの支援のもと行われたものです。
■掲載誌
Small Science, Volume 5, No. 5
掲載日:2025年5月4日
■著者
Yun Qi, Eijiro Miyako*
■論文タイトル
Multifunctional Magnetic Ionic Liquid-Carbon Nanohorn Complexes for Targeted Cancer Theranostics
■論文概要
本研究では、カーボンナノホーン表面に磁性イオン液体、近赤外蛍光色素(インドシアニングリーン)、分散剤(ポリエチレングリコール-リン脂質複合体)を被覆したナノ粒子の作製に成功しました。得られたナノ粒子は、ナノ粒子特有のEPR効果のみならず、磁性イオン液体に由来する磁場駆動の腫瘍標的能によって、大腸がんを移植したマウス体内の腫瘍内に効果的に集積し、磁性イオン液体に由来する抗がん作用に加え、生体透過性の高い近赤外レーザー光により、インドシアニングリーンに由来するがん患部の可視化とカーボンナノホーンに由来する光熱変換による多次元的な治療が可能であることを実証しました。さらに、マウスを用いた生体適合性試験などを行い、いずれの検査からもナノ粒子が生体に与える影響は極めて少ないことがわかりました。当該ナノ粒子と近赤外レーザー光を組み合わせた新たながん診断・治療技術の創出が期待されます。
表紙詳細:https://onlinelibrary.wiley.com/doi/10.1002/smsc.202570019
論文詳細:https://onlinelibrary.wiley.com/doi/full/10.1002/smsc.202400640
プレスリリース詳細:https://www.jaist.ac.jp/whatsnew/press/2025/03/06-1.html
令和7年5月8日
出典:JAIST お知らせ https://www.jaist.ac.jp/whatsnew/info/2025/05/08-2.html

