多剤耐性がんを克服する新たなナノ粒子薬物送達システムの開発に成功 ―アミノ酸由来のナノ粒子による逐次的薬物放出と光熱療法の融合ー
  |
国立大学法人東北大学 国立大学法人北陸先端科学技術大学院大学 |
多剤耐性がんを克服する新たなナノ粒子薬物送達システムの開発に成功
―アミノ酸由来のナノ粒子による逐次的薬物放出と光熱療法の融合―
【発表のポイント】
- アミノ酸を原料とした超微小粒子(ナノ粒子(注1))を独自の製法で作製し、抗がん剤をより多く効率よく詰め込むことに成功しました。
- 粒子の表面加工により、がん細胞が抗がん剤を細胞の外へ追い出す前に、その「排出ポンプ」の働きをあらかじめ止めてから抗がん剤を届ける仕組みを実現しました。
- 薬による治療とレーザー光を使った熱治療を組み合わせることで、治療が難しい多剤耐性がんのマウス実験において、40日間すべてのマウスが生存するという顕著な効果を達成しました。
- 開発したナノ粒子は正常な組織への毒性がなく、がん細胞を狙い撃ちにする機能も確認されました。
【概要】
| がん細胞が、複数の抗がん剤に対して同時に抵抗性を持つようになる現象「多剤耐性」は、がんに対する化学療法において大きな課題となっています。 東北大学 多元物質科学研究所の都英次郎教授(北陸先端科学技術大学院大学 先端科学技術研究科 客員教授)らの研究グループは、多剤耐性(注2)がんの治療に向けた革新的なナノ粒子薬物送達システムの開発に成功しました(図1)。本研究グループは、アミノ酸を原料とした超微小粒子(ナノ粒子)を独自の製法で作製し、その表面をイカやタコの墨に含まれる色素に似た物質(ポリドーパミン(注3))で層状にコーティングしました。この加工により、多剤耐性がん細胞が抗がん剤を排出する前に細胞内に蓄積させることが可能となりました。さらに、腫瘍部位を局所的に加熱する光熱療法との組み合わせにより、マウス実験で治療開始からわずか7日で腫瘍が完全に消失し、40日間すべてのマウスが副作用なく生存しました。 本成果は多剤耐性がんに対する化学療法と光熱療法を融合した新しい治療戦略として、高い臨床応用可能性を持ち、今後、様々な種類の多剤耐性腫瘍への応用拡大が期待されます。 本研究成果は、薬物送達分野の国際的権威ある学術誌「Journal of Controlled Release」に、2026年5月6日付けで掲載されました。 なお、本研究はフランス国立科学研究センター(CNRS)ストラスブール大学のAlberto Bianco博士、Cécilia Ménard-Moyon博士らの研究グループとの共同研究によるものです。 |
【詳細な説明】
研究の背景
がん化学療法における最大の障壁の一つが多剤耐性(MDR)の発現です。MDRを獲得したがん細胞は、細胞膜上にP糖タンパク質(P-gp)(注4)と呼ばれる薬物排出ポンプを過剰発現させ、投与された抗がん剤を細胞外へ積極的に排出してしまいます。その結果、薬剤の細胞内濃度が著しく低下し、治療効果が大幅に損なわれます。この問題を解決するため、P-gp阻害剤と抗がん剤を同時に投与する手法が検討されてきましたが、両薬剤が同時に放出されると、P-gpの阻害が完了する前に抗がん剤が排出されてしまうという課題がありました。
今回の取り組み
本研究グループは、チロシンおよびトリプトファンのアミノ酸誘導体を自己集合・紫外線架橋させたナノ粒子を出発材料として、独自の自己鋳型エッチング法によって多孔質アミノ酸ナノ粒子(CPP)を作製しました。この多孔質構造により、抗がん剤ドキソルビシン(Dox)(注5)を従来の非多孔質ナノ粒子(積載効率~15%、封入効率~57%)と比べて大幅に高効率で担持することが可能となりました。
次に、ナノ粒子表面にポリドーパミン(PDA)を層ごとに積層コーティングし、さらにP-gp阻害剤であるキニジン(注6)をpH感受性のイミン結合を介して表面に結合させました。この設計により、以下の3つの革新的な機能が実現されました。
1つは、逐次的薬物放出(注7)です。酸性・グルタチオン(GSH)豊富な腫瘍細胞内環境に応答して、キニジンがDoxより先に放出されます。PDAコーティング層数を3層とすることで、キニジンがP-gpを阻害した後にDoxが放出される最適な逐次放出プロファイルを実現しました。
2つ目は、光熱療法(PTT)(注8)です。PDAコーティングは近赤外線(808 nm)を吸収して熱に変換する優れた光熱変換能を示し、腫瘍部位における温度を51℃まで上昇させることが確認されました。
3つ目は、腫瘍ターゲティングです。PEGリンカーを介して表面に結合させた葉酸(FA)(注9)が、多くの腫瘍細胞で過剰発現している葉酸受容体を標的とし、ナノ粒子の腫瘍への選択的集積を促進しました。
多剤耐性EMT-6/AR1細胞を用いたin vitro実験において、本ナノ粒子(FA/C-Dox@PDA-Q)とレーザー照射を組み合わせた治療により、細胞生存率が5%未満にまで低下することが確認されました。これは化学療法単独やPTT単独の効果をはるかに超えるものです。
多剤耐性EMT-6/AR1腫瘍を移植したマウスモデルを用いたin vivo実験では、FA/C-Dox@PDA-Q+レーザー照射群において、治療開始7日後に腫瘍の完全消退が観察され、40日間の観察期間中に100%の生存率が達成されました(図2)。一方、薬剤を含まないナノ粒子(PTT単独)の群では一時的な腫瘍消退後に再発が認められ(40日生存率20%)、その他の対照群はすべて生存率0%でした。血液検査および体重モニタリングの結果から、本ナノ粒子の全身毒性がないことも確認されました。
今後の展開
本研究で開発したナノ粒子プラットフォームは、多剤耐性がんに対する化学療法と光熱療法を融合した新しい治療戦略として、高い臨床応用可能性を持ちます。今後は、様々な種類の多剤耐性腫瘍への応用拡大や、さらなる安全性・有効性の検討を進めていく予定です。

図1. 本研究の概念
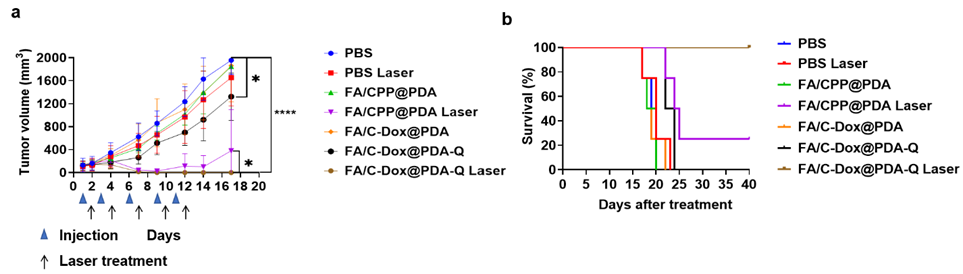
| 図2. マウスを用いた抗腫瘍効果の検証 (a) 腫瘍の大きさの変化(治療開始からの日数)4種類の条件でマウスに投与し、腫瘍の大きさを継続的に観察しました。機能性ナノ粒子(FA/C-Dox@PDA-Q)と近赤外線レーザー照射を組み合わせた群では、わずか7日間で腫瘍が完全に消失しました。一方、薬剤を含まないナノ粒子+レーザー照射の群では一時的な腫瘍消失の後に再増殖が認められ、それ以外の対照群では腫瘍の抑制効果はほとんど見られませんでした。▲印はナノ粒子の投与日、↑印はレーザー照射日を示します。 (b) 生存率(治療開始から40日間)機能性ナノ粒子(FA/C-Dox@PDA-Q)+レーザー照射を受けたすべてのマウスが、観察期間の40日間を通じて生存しました(生存率100%)。一方、他の治療条件のマウスはいずれも40日以内に全例死亡しており、本治療法の顕著な生存延長効果が示されました。 |
【謝辞】
本研究は、フランス国立科学研究センター(CNRS)、フランス国立研究機構(ANR)LabExプロジェクト(ANR-10-LABX-0026_CSC)、Jean-Marie Lehn財団、JSPS科研費 基盤研究(A)(JP23H00551)、挑戦的研究(開拓)(JP22K18440、JP25K21827)、地域中核・特色ある研究大学強化促進事業(JPMJTR22U1)、JST共創の場形成支援プログラムJPMJSF2318の支援を受けて実施されました。
【用語説明】
【論文情報】
| タイトル | Multifunctional amino acid-based nanoparticles for sequential drug delivery to overcome multidrug resistant cancer |
| 著者 | Tengfei Wang, Nina Sang, Cécilia Ménard-Moyon,* Eijiro Miyako,* Alberto Bianco* *責任著者:東北大学多元物質科学研究所 教授 都英次郎 フランス国立科学研究センター(CNRS)ストラスブール大学 Alberto Bianco博士、Cécilia Ménard-Moyon博士 |
| 掲載誌 | Journal of Controlled Release |
| DOI | 10.1016/j.jconrel.2026.114954 |
| URL | https://doi.org/10.1016/j.jconrel.2026.114954 |
令和8年5月8日
