研究活動の検索
研究概要(研究室ガイド)やプレスリリース・受賞・イベント情報など、マテリアルサイエンスの研究室により公開された情報の中から、興味のある情報をタグや検索機能を使って探すことができます。高分子化合物による細胞の凍結保護効果の機序を解明-再生組織などの長期保存技術の開発に貢献-

 |
北陸先端科学技術大学院大学 理化学研究所 |
高分子化合物による細胞の凍結保護効果の機序を解明
-再生組織などの長期保存技術の開発に貢献-
ポイント
- 高分子化合物による細胞の凍結保護効果の機序の一端を解明。
- 細胞凍結保護効果を説明するため初めて固体NMRの手法を応用し、細胞の脱水制御に伴う細胞内氷晶抑制効果を説明した。
- この手法を利用することで、新しい効果的な凍結保護物質の分子設計が可能となり、再生医療分野などへの応用が期待できる。
| 北陸先端科学技術大学院大学(学長・寺野稔、石川県能美市)先端科学技術研究科物質化学領域 松村和明教授、ラジャン・ロビン助教、理化学研究所放射光科学研究センターNMR先端応用・外部共用チーム 林文晶上級研究員、長島敏雄上級研究員らの研究グループは、高分子化合物による細胞の凍結過程における保護作用機序を明らかにした。 本研究成果は、細胞への毒性や分化への影響が低い凍結保護高分子の設計指針を明らかとすることで、再生医療分野で必要とされる幹細胞や再生組織などの効率的な凍結保存技術の開発に貢献することが期待できる。 本研究成果は、Springer Nature発行の科学雑誌「Communications Materials」誌に2021年2月9日オンライン版で公開された。なお、本研究は日本学術振興会科研費、キヤノン財団、文部科学省大学連携バイオバックアッププロジェクト、文部科学省先端研究施設共用促進事業の支援を受けて行われた。 |
【研究の背景】
医学生物学研究に必要な細胞は、細胞バンクなどから凍結状態で入手できる。細胞の凍結保存技術自体は1950年代に確立されており、おもにジメチルスルホキシド(DMSO)[*注1]が保護物質として細胞懸濁液に添加され、液体窒素温度にて凍結保存されている。一般的な樹立細胞などは既存の保存技術で問題なく保存可能な細胞が多いが、受精卵などの生殖細胞、ES細胞やiPS細胞[*注2]などの特殊な幹細胞などの中には凍結保存が困難なものが多く、効率的な保存技術の開発が望まれている。また、汎用保護剤であるDMSOは毒性があり、分化[*注3]への影響もあることから再生医療分野では代替の物質の開発が望まれているが、この半世紀ほどは新しい凍結保護物質の報告はほとんど見られなかった。高分子系の保護物質は細胞膜を容易には透過しないため、細胞への毒性や分化への影響を低くすることが可能である一方、細胞外から凍結保護を行うということから開発は困難とされてきた。2009年に松村らが両性電解質高分子[*注4]による凍結保護作用を発表し[1]、その後、多くの細胞種で凍結保護効果が確認されてきた。また、急速に凍結することで細胞内外の水の結晶化を抑制するガラス化保存技術[*注5]にも両性電解質高分子が利用され、受精卵や胚[2]や軟骨細胞シート[3]、スフェロイド[*注6] [4]などの保存に成功した。また、高分子化合物による凍結保護物質の報告は世界中で近年になって非常に多く行われており、多くの分野での応用が期待されている。しかしながら、その具体的なメカニズムはわかっていない。
【研究成果と手法】
これまでDMSOなどの低分子による細胞膜透過性の凍結保護物質については、細胞内の水の結晶化を抑制することが主な機序として報告されてきている。しかし、高分子凍結保護剤の細胞外からの保護作用の機序は詳細にはわかっておらず、最近の論文では細胞外の氷の結晶(氷晶)の成長抑制作用と説明されている。確かに氷晶は物理的に細胞を破壊するため、その抑制が重要であることは間違いがないが、一方で、細胞内に大きな氷晶が形成されることは、細胞内小器官の破壊を伴う致命的なダメージを与えるとされているため、細胞内氷晶の形成が抑制されていることが考えられる。細胞内氷晶の形成については、一般的には顕微鏡などで観察されるが、凍結時の細胞内の現象を正確に捉えることが難しいため、はっきりしたことは分からない状況であった。
研究グループらは、両性電解質高分子溶液の凍結保護の分子メカニズムを調べるため、固体NMR[*注7]の手法を初めて応用し、凍結保護という複雑かつ多面的な現象の特徴を塩や水、高分子の運動と状態からの視点で解き明かすことに成功した。
両性電解質高分子であるカルボキシル基導入ポリリジン(PLL-(0.65) (図1))溶液、比較対象として、凍結保護効果の高いDMSO溶液、凍結保護効果のあまり見られないアルブミン(BSA)溶液、ポリエチレングリコール(PEG)溶液、保護効果のない生理的食塩水について、0℃から-41℃までの水分子および塩(イオン)の運動性を固体NMR測定により評価した。その結果、低温時の水の運動性がPLL-(0.65)溶液において他の溶液に比べ顕著に抑制され粘性が上昇することがわかった(図2)。凍結条件下では、この粘性の高いポリマー溶液が細胞の周辺を取り囲むことにより、細胞内への氷晶の侵入による細胞内氷晶形成を抑制していることが示唆される。また、PLL-(0.65)溶液中では高分子鎖にNaイオンがトラップされ、低温域でのNaイオンの運動性が低下していることも確認された(図3)。これにより、浸透圧に寄与するNaイオンの濃度がPLL(0.65)溶液において低下し、急激な脱水を抑制し、温和な条件でかつ十分に細胞内を脱水できる最適条件を達成していることが細胞内氷晶の形成の抑制を示唆する結果となった。これらの機序を図4に模式図として表す。低温時に高分子が塩や水を包含した会合体を形成し、それらの運動性が低下することで温和な条件でかつ十分に脱水が起こると共に、細胞外溶液の粘性の上昇に伴う細胞外氷晶の成長も抑えられ、結果的に細胞内氷晶の形成が抑制されることが細胞の凍結保護を可能としていることが考えられる。この機序は細胞内に浸透する既存の凍結保護剤と異なることから、新たな機序に基づく凍結保護剤の開発につながる研究成果である。
【今後の展開】
固体NMR測定により高分子や塩、水の分子運動の観点から細胞凍結保護高分子の新規機序について考察することが可能となった。この手法により効果の高い凍結保護剤の設計指針が得られることが期待される。また、細胞だけでなく、再生組織などの2次元3次元の生体組織などの効率的な保存法、保存剤の開発に役立つことが期待できる。

図1 本研究で使用した両性電解質高分子であるカルボキシル化ポリリジンの構造。PLL-(0.65)は、コハク酸付加部位(m)が65%であるものを示す。 |

図2 1H NMRの水のピーク幅の温度依存性。PLL-(0.65)に顕著な広幅化が見られ、低温での粘性の急上昇が確認された。 |
 図3 a) 23Na NMRのピーク面積から、各溶液中の凍結下、氷と共存する溶液状態にあるNaイオンの量を評価した。凍結下のPLL-(0.65)溶液において、溶液として振舞うNaイオンの量が低下した。b)Naイオン量から系中のNaCl濃度を計算した結果。PLL-(0.65)溶液中のNaCl濃度は温度低下と共に速やかに上昇し、低温下で緩やかに下降する。これは速やかかつ適度な細胞の脱水による細胞内氷晶形成の抑制を示唆している。 |
 図4 PLL-(0.65)溶液による細胞の凍結保護効果の模式図。低温凍結下、1) 高分子が高い粘性を持つ会合体(マトリックス)を形成することで、細胞外からの氷核の流入を阻止し、2) 塩や水をマトリクス内にトラップすることにより、凍結後の脱水を温和な条件で制御するという2つの効果で細胞内の氷晶形成を抑制している。また、マトリックス形成による粘度上昇は、氷晶が細胞膜を刺激する事による細胞内氷晶形成も抑制していることが示唆された。 |
【参考文献】
[1] Matsumura K, Hyon SH, Polyampholytes as low toxic efficient cryoprotective agents with antifreeze protein properties. Biomaterials 30, 4842-4849 (2009)
[2] Kawasaki Y, Kohaya N, Shibao Y, Suyama A, Kageyama A, Fujiwara K, Kamoshita M, Matsumura K, Hyon S-H, Ito J, Kashiwazaki N. Carboxylated ε-poly-L-lysine, a cryoprotective agent, is an effective partner of ethylene glycol for the vitrification of embryos at various preimplantation stages. Cryobiology, 97, 245-249 (2020)
[3] Hayashi A, Maehara M, Uchikura A, Matsunari H, MatsumuraK, Hyon SH, Sato M, Nagashima H. Development of an efficient vitrification method for chondrocyte sheets for clinical application. Regenerative Therapy, 14, 215-221 (2020)
[4] Matsumura K, Hatakeyama S, Naka T, Ueda H, Rajan R, Tanaka D, Hyon SH. Molecular design of polyampholytes for vitrification-induced preservation of three-dimensional cell constructs without using liquid nitrogen. Biomacromolecules, 21, 3017-3025 (2020)
【用語解説】
注1 ジメチルスルホキシド(DMSO)
分子式C2H6SOの有機溶媒の一種。実験室レベルから工業的規模に至るまで広く溶媒として使用される他、10%程度の溶液は細胞の凍結保存として使用されている。
注2 ES細胞やiPS細胞
多能性幹細胞の一種。ES細胞は胚性幹細胞、iPS細胞は人工多能性幹細胞の略である。生体外にて、理論上ほぼすべての組織に分化する分化多能性を保ちつつ、ほぼ無限に増殖させることができるため、有力な万能細胞の一つとして再生医療への応用が期待されている。現在はDMSOを使用した保存液で保存されているが、DMSOの分化への影響が危惧される。
注3 分化
多細胞生物において、個々の細胞が構造機能的に変化すること。
注4 両性電解質高分子
一分子中にプラスとマイナスの電荷を共にもつ高分子化合物。
注5 ガラス化保存技術
受精卵などの保存によく用いられている超低温保存の一つ。凍結時においても氷の結晶を形成しにくい溶質濃度の高いガラス化液を用い、保存した細胞が氷による物理的傷害を受けにくい。
注6 スフェロイド
三次元的な細胞のコロニーで、再生医療の組織形成のビルディングブロックとして期待されている。
注7 固体NMR
固体NMRとは固体試料を観測対象とした核磁気共鳴 (NMR) 分光法で、方向依存的な異方性相互作用の存在のため共鳴線の線幅が広いのが特徴である。通常、共鳴線の先鋭化のため、試料を静磁場に対してマジック角(54.7°)傾けて、超高速で回転(MAS:Magic Angle Spinning)させて測定を行う。本研究では、温度制御装置を備え付けた固体MAS検出器により、プロトンとナトリウムの核磁気共鳴スペクトルを測定し、低温時の水やNaイオン、高分子の運動性について議論した。
【論文情報】
| 掲載誌 | Communications Materials(Springer Nature) |
| 論文題目 | Molecular mechanisms of cell cryopreservation with polyampholytes studied by solid-state NMR |
| 著者 | Kazuaki Matsumura, Fumiaki Hayashi, Toshio Nagashima, Robin Rajan,Suong-Hyu Hyon |
| 掲載日 | 2021年2月9日10時(英国時間)にオンライン版に掲載 |
| DOI | 10.1038/s43246-021-00118-1 |
令和3年2月9日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2021/02/post_588.htmlNEDO「ムーンショット型研究開発事業」研究開発プロジェクトに採択
 |
国立大学法人北陸先端科学技術大学院大学 |
|
このたび、北陸先端科学技術大学院大学(学長・寺野 稔、石川県能美市)ら8機関による提案研究が、国立研究開発法人新エネルギー・産業技術総合開発機構(NEDO)の「ムーンショット型研究開発事業※」におけるムーンショット目標4「2050年までに、地球環境再生に向けた持続可能な資源循環を実現」の達成を目指す研究開発プロジェクトに採択されました。
1)ON型光スイッチ:陸域の生活圏では材料として安定ですが、投棄後に海洋流出するまでの過程で生じる表面損傷などにより太陽光がプラスチック内部に届き生分解が始まる(ON)スイッチです。 2)OFF型光スイッチ:蛍光灯や太陽光暴露のある状態では生分解が抑制(OFF)され、海中・海底・コンポストなどの暗所の環境で生分解が始まるという「光スイッチ」です。 3)また、これらを具有させたON/OFF型という理想的システムも同時に提案します。 さらには、海洋生物が誤飲したり周りまわって人間の食料中に混ざり込んでも消化管内で物理的障害や化学的毒性を生じない「食せるプラスチック」の開発も目指します。 2030年にはこれらの海洋実環境における分解性を証明し衣料品やビニール袋などの試作品を作製します。さらに、上記のシステムは広範囲のプラスチックに適用できるため、2050年までにはさらに多くのプラスチックへと展開し様々な種類や形態の光スイッチ型分解性プラスチック製品へと展開します。本プロジェクトは、二酸化炭素の固定化、炭素循環および窒素循環などの概念を取り入れた統合的な地球環境保全・再生に資するものです。加えて、本プロジェクトは、成熟期に差し掛かってきた我が国の石油化学産業をバイオ化学産業に業態転換せしめ、新たな成長に向けたパラダイムチェンジ型イノベーションの一端を担う可能性を有します。 |
<参 考>
1 ムーンショット型研究開発制度
本制度の詳細については、以下を参照
https://www8.cao.go.jp/cstp/moonshot/index.html
2 ムーンショット目標
2020年1月CSTIにおいてムーンショット目標1~6が決定。2020年7月には健康・医療戦略推進本部においてムーンショット目標7が決定
目標1:2050年までに、人が身体、脳、空間、時間の制約から解放された社会を実現
目標2:2050年までに、超早期に疾患の予測・予防をすることができる社会を実現
目標3:2050年までに、AIとロボットの共進化により、自ら学習・行動し人と共生するロボットを実現
目標4:2050年までに、地球環境再生に向けた持続可能な資源循環を実現
目標5:2050年までに、未利用の生物機能等のフル活用により、地球規模でムリ・ムダのない持続的な
食料供給産業を創出
目標6:2050年までに、経済・産業・安全保障を飛躍的に発展させる誤り耐性型汎用量子コンピュータを実現
目標7:2040年までに、主要な疾患を予防・克服し100歳まで健康不安なく人生を楽しむための
サステイナブルな医療・介護システムを実現
3 NEDOムーンショット型研究開発事業の採択結果
https://www.nedo.go.jp/news/press/AA5_101346.html
令和2年9月7日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2020/09/7-1.html多糖が自らパーティション -光合成産物の多糖が乾燥下、センチメートルスケールの3次元空間を認識-

多糖が自らパーティション
-光合成産物の多糖が乾燥下、センチメートルスケールの3次元空間を認識-
PRポイント
- 「多糖が乾燥環境下、3次元空間を認識することを世界で初めて発見」
- 「乾燥によって析出した多糖の薄膜はナノメーターから階層的に整った構造で、新たなバイオマテリアルの設計手法が期待」
- 「天然高分子への展開」:今回、淡水性シアノバクテリア由来の多糖類を使用したin vitro実験によって新現象が確認されており、今後、他の多糖や天然高分子などでも展開を検討
|
北陸先端科学技術大学院大学(学長・浅野哲夫、石川県能美市)、環境・エネルギー領域の桶葭興資助教、金子達雄教授らは、シアノバクテリア由来の多糖が自ら乾燥環境でセンチメートルスケールのパターンを形成することを発見した。多糖と乾燥環境は自然界で密接な関係にあり、今回のin vitro実験で「多糖が空間を認識する能力」が実証されただけでなく、簡便な乾燥によってバイオマテリアルの新たな設計手法が見出されると期待される。 自然界では熱帯魚の縞模様や巻貝のらせんなど様々な幾何学模様がセンチメートル以上のスケールで存在し、パターン発生原理の議論は歴史的研究の一つである。例えば、人工的に化学物質を選択してチューリングパターンやベローソフ・ジャボチンスキー反応など、パターン発生原理の研究が世界的に何世紀にも渡ってなされてきた。しかし、「自然界にある物理化学的な条件を再現して人工的にパターンを制御すること」はこれまで困難を極めていた。 これに対して研究チームは今回、シアノバクテリア由来の多糖が乾燥環境下、センチメートルスケールで空間分割パターンを形成することを発見した。多糖の水溶液を狭い間隙の制限空間から乾燥させると、1つの空間を複数の空間に分けるように多糖が析出する(図)。蒸発時、多糖は気液界面を増加させようとして界面を分割して薄膜として析出した。このように空間がパーティション化される現象はin vitro実験で確認されたもので、自然環境の多糖が乾燥と常に対面していることと密接に関係する。特に、今回使用した多糖は、シアノバクテリアが光合成によって生み出したサクランという生体適合性に優れた物質を用いているため、再生医療用材料としても有望である。
本成果は、英国科学雑誌「Scientific Reports」誌に7/21午前10時(英国時間)オンライン版で公開された。 |
<論文情報>
掲載誌:Scientific Reports
論文題目:Emergence of polysaccharide membrane walls through macro-space partitioning via interfacial instability.
著者:Kosuke Okeyoshi, Maiko K. Okajima, Tatsuo Kaneko
DOI: 10.1038/s41598-017-05883-z
掲載日:7月21日午前10時(英国時間)にオンライン掲載
|
本研究成果は、以下の事業・開発課題によって得られました。 |
<背景と経緯>
建築学で駆使されている3次元的な幾何構造は、自然対数を利用した橋の設計など自然界と調和した形状である。材料学においても自然界と調和する幾何形状や規則性の制御によって新しい材料設計方法が期待され続けている。しかし、「自然界にある物理化学的な条件下を再現して人工的に幾何学パターンを制御すること」はこれまで困難を極めていた。
自然界では熱帯魚の縞模様や巻貝のらせんなど様々な幾何学模様がセンチメートル以上のスケールで存在し、パターン発生の議論は歴史的研究の一つである。例えば、人工的に化学物質を選択してチューリングパターン注1)やベローソフ・ジャボチンスキー反応注2)など、パターン発生原理の研究が世界的になされてきた。さて、生物の体表などのパターンはなぜできるのか?遺伝子?天気?それとも..?果たして「人工的な実験」で、「ビーカーの中」で、科学によって再現できるのか?
<今回の成果>
1.乾燥環境下で多糖が3次元空間を認識することを発見(図1)
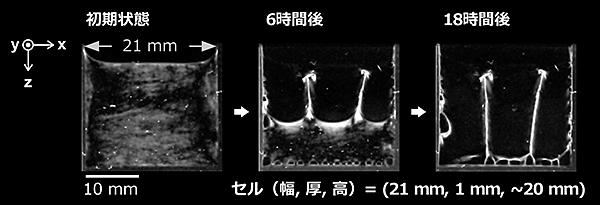
乾燥環境下、シアノバクテリア注3)由来の多糖注4)がセンチメートルスケールの3次元空間を認識して、自らパーティションとなるように析出膜を形成することを発見した。この現象はin vitro注5)実験で確認されたもので、高粘性の多糖「サクラン」注6)の水溶液を2枚のガラス板に挟まれた間隙の制限空間から乾燥させると、1つの空間を複数の空間に分けるように多糖が析出する。
初期状態:間隙1 mmの上面開放型セルに多糖の水溶液を満たす。セルの幅をセンチメートルスケールで様々に変えて乾燥実験を行った。
乾燥過程:セルの幅が0.7 cm 程度であると、2枚のガラス板を橋掛けするような析出膜は形成されず、底に析出するだけであった。これに対して、1.5 cm 容器の幅を広げると、2枚のガラス板を橋掛けするような析出膜が形成された。高分子のサイズからすれば、1 mm の間隙は著しく大きいにもかかわらず、橋掛けできることは驚異に値する。これは、多糖が自己集合的に20 µm以上の長さのファイバー状となっていることが関係する。さらにセルの幅を広げると垂直に析出する膜の数は増え、3次元空間が複数に分けられた。幅が10 cmの場合でもこの現象は確認され、多糖が乾燥時に自らパーティションとなる析出膜を形成し、センチメートル空間を認識可能であることを裏付けている。
2.垂直に析出した膜は、高分子がナノメータースケールから3次元的に揃っている(図2)
さらに、この析出膜を偏光顕微鏡や電子顕微鏡で観察すると、2枚のガラス板を結ぶ方向に、高分子が整然と揃っていることが判明した。多糖の水溶液を乾燥するだけで高分子が3次元的に方向制御されることは極めて驚異である。
この析出膜に架橋構造を導入したあと水に再び戻すと、遮光用ブラインドのように一方向に大きく伸びる。図2中の青いまま伸びている様子は、高分子の3次元的な整列を保ったまま一方向に伸びていることを示す。
なお、研究チームはこれまでにも、層状構造を持つ膜から一次元膨潤するゲルの作製に成功している。今回の新たな膜作製技術と合わせてバイオマテリアルへの応用が期待できる。
<今後の展開>
パーティション現象を他の天然高分子へ展開
物理化学的な条件と幾何学的な条件を整えることで、他の多糖や高分子へ展開可能である。特に「乾燥環境」に注目して、パターンの形成法則を系統的に解明することで、陸上進出する多糖の進化を紐解けるかもしれない。
パターンが多糖で構成されているため、新たなバイオマテリアル設計手法が期待される
センチメートル以上の空間パターンを自発的に形成する構造には、リーゼガング現象やチューリング現象など自己組織化による「散逸構造」が挙げられる。しかしこれらの現象は、生体が存在し得る自然界の物理化学条件から遠く離れた環境でのみ可能で、材料分野への適用は困難を極めていた。
一般に、多糖、DNAおよび骨格タンパク質などの剛直な生体高分子はナノメートルやマイクロメートルスケールのパターンを形成することが知られている。ポリペプチドのαヘリックスやβシート、DNAの螺旋構造はその代表例である。これに対して研究チームが発見したパーティション現象は、光合成産物の多糖を使って発見したセンチメートルスケールの空間パターンであり、散逸構造を用いた材料学の道が一気に開かれる。さらに、DDSなど医療用材料に期待の大きい多糖を使用していることから、臓器の再生医療などに向けた新たな材料設計手法として有望である。
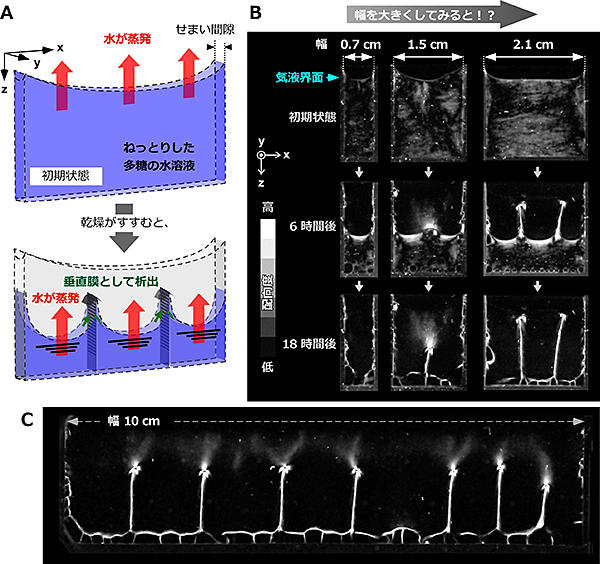
図1. 多糖の乾燥実験とパーティション現象
A. 上面開放型セルから多糖の水溶液を乾燥させる実験の概念図。
B. 様々な幅からの乾燥過程を2枚の偏光子を介して観察した画像。白色部分は高分子が配向している(揃っている)。
C. 幅10 cmの上面開放型セルから乾燥させたあとに現れる空間分割パターン。

図2. 析出した垂直膜の顕微鏡観察と瞬時に一方向へ膨らむゲル
乾燥実験後に析出した垂直膜を特殊な光学フィルターが入った偏光顕微鏡で観察すると、2枚のガラス板を結ぶ方向に高分子が整然と配向していることが分かる。さらにこの乾燥した膜を水にもどすと、「窓のブラインド」のように瞬時に一方向へ膨らむことが分かった。
<用語解説>(Wikipedia より)
注1)チューリングパターン:
イギリスの数学者アラン・チューリングによって1952年に理論的存在が示された自発的に生じる空間的パターンである。
注2)ベローソフ・ジャボチンスキー反応:
系内に存在するいくつかの物質の濃度が周期的に変化する非線型的振動反応の代表的な例として知られている。この反応などの振動反応は平衡熱力学の理論が成り立たない非平衡熱力学分野の代表例である。
注3)シアノバクテリア:
ラン藻細菌のこと。光合成によって酸素と多糖を生み出す。
注4)多糖:
グリコシド結合によって単糖分子が多数重合した物質の総称である。デンプンなどのように構成単位となる単糖とは異なる性質を示すようになる。広義としては、単糖に対し、複数個(2分子以上)の単糖が結合した糖も含むこともある。
注5)in vitro:
"試験管内で"という意味で、試験管や培養器などの中でヒトや動物の組織を用いて、体内と同様の環境を人工的に作り、薬物の反応を検出する試験のことを指す。in vitroの語源はラテン語で「ガラスの中で」という意味。
注6)サクラン:
硫酸化多糖類の一つで、シアノバクテリア日本固有種のスイゼンジノリ (学名:Aphanothece sacrum) から抽出され、重量平均分子量は2.0 x 107g/mol とみつもられている。
平成29年7月21日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2017/07/21-1.html磁石と光で機能制御可能なナノ粒子の開発に成功! -高性能がん診断・治療に向けて-
磁石と光で機能制御可能なナノ粒子の開発に成功!
-高性能がん診断・治療に向けて-
【ポイント】
- 磁性イオン液体とカーボンナノホーンから成る複合体の作製に成功
- 当該ナノ粒子の磁場応答性とEPR効果により標的とする腫瘍内に効果的に集積し、マウスに移植したがんの可視化と、抗がん作用、光熱変換によるがん治療が可能であることを実証
- 当該ナノ粒子と近赤外光を組み合わせた新たながん診断・治療技術の創出に期待
| 北陸先端科学技術大学院大学(学長・寺野 稔、石川県能美市)物質化学フロンティア研究領域の都 英次郎教授らは、カーボンナノホーン*1表面に磁性イオン液体*2、近赤外蛍光色素(インドシアニングリーン*3)、分散剤(ポリエチレングリコール-リン脂質複合体*4)を被覆したナノ粒子の作製に成功した(図1)。得られたナノ粒子は、ナノ粒子特有のEPR効果*5のみならず、磁性イオン液体に由来する磁場駆動の腫瘍標的能によって、大腸がんを移植したマウス体内の腫瘍内に効果的に集積し、磁性イオン液体に由来する抗がん作用に加え、生体透過性の高い近赤外レーザー光*6により、インドシアニングリーンに由来するがん患部の可視化とカーボンナノホーンに由来する光熱変換による多次元的な治療が可能であることを実証した。さらに、マウスを用いた生体適合性試験などを行い、いずれの検査からもナノ粒子が生体に与える影響は極めて少ないことがわかった。当該ナノ粒子と近赤外レーザー光を組み合わせた新たながん診断・治療技術の創出が期待される。 |
【研究背景と内容】
がんは世界における死亡の主な原因の1つである。世界保健機関 (WHO) によると、2020年には約1,000万人のがん患者が亡くなっている。とりわけ先進国の人口の高齢化と生活習慣の要因により、症例数は引き続き増加すると予想されている。科学、技術、社会の発展が大きく進歩したにもかかわらず、従来の抗がん剤の特異性の低さ、重篤な副作用、転移性疾患に対する有効性の限界などが相まって、がんは依然として重要かつ世界的な健康課題となっている。従って、より効果的かつ安心・安全な先進がん診断・治療技術の開発は急務である。
イオン液体は、低融点、低揮発性、高イオン濃度、高イオン伝導性などの特長を持つ室温で液体として存在する塩であり、コンデンサ用電解液や帯電防止剤、CO2吸収剤などの様々な産業用途に応用されており、とりわけ環境・エネルギー分野で注目されている。また、近年イオン液体に抗がん作用があることが見出されており、上記の分野のみならず医療分野への応用展開も期待されている。
そもそもイオン液体という物質は、陽イオン分子と陰イオン分子という極めてシンプルな2種類の構成要素で成り立っている。つまり、陽イオン側と陰イオン側の両方に多様な可能性があることから、両者の組み合わせとなるイオン液体には、膨大な種類が存在しうることになる。そのためイオン液体は「デザイナー溶媒」と呼ばれている。例えば、陽イオンが1-ブチル-3-メチルイミダゾリウム、陰イオンが塩化鉄であるイオン液体([Bmin][FeCl4])は、ネオジム磁石程度の磁場に応答する「磁性イオン液体」として知られている。磁石に反応する流体としては、この磁性イオン液体の他に、磁性流体という粉末磁石を懸濁させた油などが知られている。しかし、従来の磁性流体は、固体と液体に分離してしまいやすく不安定であった。磁性イオン液体は極めて安定であり、揮発せず、燃えないなどのイオン液体特有の性質を保持している。このため磁性イオン液体は、固体磁石にはできなかった液体磁石の新しい用途に向けて応用が期待されている。しかし、このような磁性イオン液体の高い潜在能力に反して、これまで報告されている磁性イオン液体の応用例は、化学物質の抽出や分離に限られていた。
一方、ナノ炭素材料の一つであるカーボンナノホーン(CNH)は、高い生体適合性と優れた物理化学的特性を有することが知られており、とりわけバイオメディカル分野で大きな注目を集めている。都教授は、CNHが生体透過性の高い波長領域(650~1100 nm)のレーザー光により容易に発熱する特性(光発熱特性)を世界に先駆けて発見し、当該光発熱特性を活用したがん診断・治療技術の開発を推進している(※1)。また、都研究室では、革新的がん診断・治療技術に向けてCNHのさらなる高性能化・高機能化に取り組んでいる(※2)。
(※1) https://www.jaist.ac.jp/whatsnew/press/2020/08/17_2.html
(※2) https://www.jaist.ac.jp/whatsnew/press/2024/08/22-1.html
本研究では、磁性イオン液体([Bmin][FeCl4])と光発熱素材(CNH)を複合化した新規ナノ粒子を開発し、がん診断・治療技術への可能性を調査した。より具体的には、[Bmin][FeCl4]、近赤外蛍光色素(インドシアニングリーン)、分散剤(ポリエチレングリコール-リン脂質複合体)を被覆したCNH([Bmin][FeCl4]‒PEG‒ICG‒CNH複合体)をがん患部に同時に送り込むことで、[Bmin][FeCl4]に由来する磁場応答性と抗がん作用に加え、生体透過性の高い近赤外レーザー光を用いることで、インドシアニングリーンに由来する近赤外蛍光特性を用いた患部の可視化やCNHに由来する光熱変換を利用した、新たながんの診断や治療の実現を目指した。
当該目標を達成するために、今回開発した技術では、簡便な超音波照射によって[Bmin][FeCl4]、近赤外蛍光色素(インドシアニングリーン)、ポリエチレングリコール-リン脂質複合体をCNH表面に吸着させることで、CNHを水溶液中に分散できるようにした(図1)。この方法で作製した[Bmin][FeCl4]‒PEG‒ICG‒CNH複合体は、7日以上の粒径安定性を有していること、細胞に対し高い膜浸透性を有し抗がん作用を発現すること、近赤外レーザー光照射により発熱が起こることが確認できたため、がん患部の可視化と治療効果について試験を行った。
大腸がんを移植して約10日後のマウスに、当該[Bmin][FeCl4]‒PEG‒ICG‒CNH複合体を尾静脈から投与し、医療用バンデージを使って患部に小型のネオジウム磁石を24時間張り付けた後に740~790 nmの近赤外光を当てたところ、がん患部が蛍光を発している画像が得られた(図2A)。また、当該ナノ粒子が、ネオジウム磁石を用いない場合や磁性イオン液体を被覆していないナノ粒子(PEG‒ICG‒CNH複合体)に比較して、がん組織に効果的に取り込まれていることが分かった(図2A)。そこで、当該ナノ粒子([Bmin][FeCl4]‒PEG‒ICG‒CNH複合体 + 磁場)が集積した患部に対して808 nmの近赤外レーザー光を照射したところ、[Bmin][FeCl4]に由来する抗がん作用に加え、CNHの光熱変換による効果で5日後には、がんを完全に消失させることが判明した(図2B)。
一方、腫瘍内における薬効メカニズムを組織学的評価により調査したところ、とりわけ磁場印可とレーザー照射した[Bmin][FeCl4]‒PEG‒ICG‒CNH複合体においてがん細胞組織の顕著な破壊が起こることが明らかとなった。
さらに、[Bmin][FeCl4]‒PEG‒ICG‒CNH複合体をマウスの静脈から投与し、生体適合性を組織学的検査、血液検査、体重測定により評価したが、いずれの項目でも[Bmin][FeCl4]‒PEG‒ICG‒CNH複合体が生体に与える影響は極めて少ないことがわかった。
これらの成果は、今回開発した[Bmin][FeCl4]‒PEG‒ICG‒CNH複合体が、革新的がん診断・治療法の基礎に成り得ることを示すだけでなく、ナノテクノロジーや光学といった幅広い研究領域における材料設計の技術基盤として貢献することを十分期待させるものである。
本成果は、2025年3月3日に生物・化学系のトップジャーナル「Small Science」誌(Wiley発行)のオンライン版に掲載された。なお、本研究は、文部科学省科研費 基盤研究(A)(23H00551)、文部科学省科研費 挑戦的研究(開拓)(22K18440)、国立研究開発法人科学技術振興機構(JST) 研究成果最適展開支援プログラム (A-STEP)(JPMJTR22U1)、大学発新産業創出基金事業スタートアップ・エコシステム共創プログラム(JPMJSF2318)ならびに本学超越バイオメディカルDX研究拠点、本学生体機能・感覚研究センターの支援のもと行われたものである。
 図1.様々な機能性分子を被覆したナノ粒子の作製と本研究の概念。
図1.様々な機能性分子を被覆したナノ粒子の作製と本研究の概念。
CNH: カーボンナノホーン、ICG: インドシアニングリーン、[Bmim][FeCl4]: 磁性イオン液体、
DSPE‒PEG2000‒NH2: ポリエチレングリコール-リン脂質複合体。
 図2. ナノ粒子をがん患部に集積・可視化(A)し、光照射によりがんを治療(B)
図2. ナノ粒子をがん患部に集積・可視化(A)し、光照射によりがんを治療(B)
(赤色の囲いは腫瘍の位置、赤色の矢印は消失した腫瘍の位置をそれぞれ示している)。
【論文情報】
| 掲載誌 | Small Science |
| 論文題目 | Multifunctional magnetic ionic liquid-carbon nanohorn complexes for targeted cancer theranostics |
| 著者 | Yun Qi, Eijiro Miyako* |
| 掲載日 | 2025年3月3日にオンライン版に掲載 |
| DOI | 10.1002/smsc.202400640 |
【用語説明】
飯島澄男博士らのグループが1998年に発見したカーボンナノチューブの一種。直径は2~5 nm、長さ40~50 nmで不規則な形状を持つ。数千本が寄り集まって直径100 nm程度の球形集合体を形成している。とりわけ、薬品の輸送用担体として期待されており、バイオメディカル分野で注目を集めている。
磁気力によってイオンが移動する液体。
肝機能検査に用いられる緑色色素のこと。近赤外レーザー光を照射すると近赤外蛍光と熱を発することができる。
ポリエチレングリコールとリンを含有する脂質(脂肪)が結合した化学物質。脂溶性の薬剤を可溶化させる効果があり、ドラッグデリバリーシステムによく利用される化合物の一つ。
100nm以下のサイズに粒径が制御された微粒子は、正常組織へは漏れ出さず、腫瘍血管からのみ、がん組織に到達して患部に集積させることが可能である。これをEPR効果(Enhanced Permeation and Retention Effect)という。
レーザーとは、光を増幅して放射するレーザー装置、またはその光のことである。レーザー光は指向性や収束性に優れており、発生する光の波長を一定に保つことができる。とくに700~1100 nmの近赤外領域の波長の光は生体透過性が高いことが知られている。
令和7年3月6日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2025/03/06-1.html学生の鈴木さんがeMEDX-24においてOutstanding Student Poster Awardを受賞
学生の鈴木超さん(博士後期課程1年、物質化学フロンティア研究領域、松村研究室)が、International Symposium on Exponential Biomedical DX 2024(eMEDX-24)においてOutstanding Student Poster Awardを受賞しました。
eMEDX-24は令和6年12月19日~20日にかけて石川県にて開催されたバイオマテリアルとDXの融合に関する国際会議です。同会議では、ウェルビーイングの実現に貢献することに重点を置き、高分子やナノマテリアルなどの材料とコンピューターサイエンスの融合による医療材料研究に関する最新の研究成果について議論が行われました。
※参考:eMEDX-24
■受賞年月日
令和6年12月20日
■研究題目、論文タイトル等
Synthesis and Evaluation of Donor-Acceptor Conjugated Polymers for Thermo-responsive Protein DDS
■研究者、著者
鈴木超、松村和明
■受賞対象となった研究の内容
温度応答性の高分子を用いたドラッグデリバリーシステム(DDS)のための生体内での発熱源として、近赤外光を吸収して発熱するドナーアクセプター(DA)高分子の合成を行いました。このDAポリマーをナノ粒子化することに成功し、808nmの近赤外光を照射することで速やかな発熱を確認しました。今後はこのポリマーナノ粒子と温度応答性高分子を組み合わせることで、近赤外光に応答した薬物放出可能なDDSの創出に取り組んでいきます。
■受賞にあたって一言
今回、Outstanding Student Poster Awardを受賞することができ、大変光栄です。国内外の研究者、学生の方々から様々な質問をいただき、とても刺激的な機会となりました。これからもより一層研究に励みたいと思います。
令和7年1月31日
出典:JAIST 受賞https://www.jaist.ac.jp/whatsnew/award/2025/01/31-1.htmlInternational Symposium on Exponential Biomedical DX 2024を開催
2024年12月19日から20日にかけて、本学 超越バイオメディカルDX研究拠点主催の第1回国際シンポジウム「International Symposium on Exponential Biomedical DX 2024(eMEDX-24)」を石川ハイテク交流センターにて開催しました。本シンポジウムでは、「ウェルビーイングの実現」をテーマに、バイオメディカルサイエンス・テクノロジーの最前線で活躍する国内外の研究者・科学者が一堂に会し、多岐にわたるテーマについて自由闊達な議論が展開されました。参加者は総勢148名に上り、基調講演4件、特別講演9件、招待講演32件が行われました。
本学の寺野 稔 学長および大会長である超越バイオメディカルDX研究拠点長の松村 和明 教授による開会挨拶の後、東京女子医科大学 岡野 光夫 名誉教授と亜洲大学校 キ・ドン・パク 教授による基調講演が行われました。岡野名誉教授は温度応答性高分子材料の研究、パク教授は生理活性ヒドロゲルの研究について、それぞれ医療分野への応用を含めた最先端の成果を発表し、参加者の大きな関心を引きました。続いて、バイオメディカル分野で活躍するトップランナーの研究者による特別講演や招待講演が行われ、参加者同士の活発な意見交換が展開されました。また、北陸三県のバイオメディカル研究室に所属するJST次世代研究者挑戦的研究プログラム(SPRING)に採択された博士後期課程の学生が主催する特別セッションでは、博士号取得後のキャリアプランについて熱心な議論が交わされました。
二日目には、京都大学 秋吉 一成 名誉教授と韓国科学技術研究院 クァン・リョル・リー 博士による基調講演が行われました。秋吉名誉教授はバイオインスパイアードナノマテリアルを活用したドラッグデリバリーシステムの開発について、また、リー博士はマテリアルズR&Dデータにおけるスキーマおよび語彙の標準化に関する研究成果について講演されました。その後、バイオメディカル分野を牽引する第一線の研究者による特別講演や招待講演が続き、参加者間では熱心な議論や意見交換が行われました。また、国内外の学生による最新の研究に関するポスター発表(49件)が行われ、活発なディスカッションが繰り広げられました。その結果、4名の学生が最優秀学生ポスター賞を、8名の学生が優秀学生ポスター賞を受賞し、授賞式が執り行われました。その後、本学超越バイオメディカルDX研究拠点の栗澤 元一 教授および都 英次郎 教授による挨拶で締めくくられ、盛況のうちに終了しました。
本シンポジウムの開催を契機に、ウェルビーイングの実現に向けて、超越バイオメディカルDX研究のさらなる加速を目指して邁進してまいります。


開会の挨拶をする寺野 稔 学長(左)と
松村 和明 超越バイオメディカルDX研究拠点長

基調講演①
岡野 光夫 名誉教授
(東京女子医科大学)

基調講演②
キ・ドン・パク 教授
(亜州大学校)

基調講演③
秋吉 一成 名誉教授
(京都大学)

基調講演④
クァン・リョル・リー 博士
(韓国科学技術研究院)

SPRING主催特別セッション

ポスター発表

優秀学生ポスター賞受賞式


閉会の挨拶をする栗澤 元一 教授(左)と
都 英次郎 教授(右)

シンポジウムの様子
令和6年12月27日
出典:JAIST お知らせ https://www.jaist.ac.jp/whatsnew/info/2024/12/27-1.html大学見本市2024~イノベーション・ジャパンに本学が出展
8月22日(木)・23日(金)の2日間、東京ビッグサイト(東京都江東区有明)で国内最大規模の産学マッチングイベントである「大学見本市2024~イノベーション・ジャパン」が開催されます。
本学からは大学等シーズ展示に松見教授、JST採択課題出展ブースに栗澤教授が出展します。
ご来場の際にはぜひお立ち寄りください。
| 日 時 | 8月22日(木) 10時00分~17時00分 8月23日(金) 10時00分~17時00分 |
| 会 場 | 東京ビッグサイト 南展示棟 南1ホール(東京都江東区有明3丁目11番1) |
| 大学等 シーズ展示 |
先端科学技術研究科 融合科学共同専攻 松見 紀佳 教授 【小間番号】 C-024 |
| JST採択課題 出展ブース (A-STEP) |
先端科学技術研究科 物質化学フロンティア研究領域 栗澤 元一 教授 【小間番号】J-019 |
詳細はこちらをご覧ください。
・大学見本市2024~イノベーション・ジャパン公式サイト
https://innovationjapan.jst.go.jp/
統合失調症の認知機能障害を回復する新薬候補 -脳移行性の皮下投与型ペプチドナノ製剤を開発-
   |
| 国立大学法人 国立大学法人広島大学 国立大学法人大阪大学 国立大学法人筑波大学 一丸ファルコス株式会社 |
統合失調症の認知機能障害を回復する新薬候補
-脳移行性の皮下投与型ペプチドナノ製剤を開発-
【ポイント】
- 統合失調症の発症に関係する神経ペプチド受容体VIPR2に対する選択的な阻害ペプチドKS-133と脳移行性のLRP1結合ペプチドKS-487を同時に搭載するナノ粒子を創製し、 皮下投与型のペプチド製剤として開発
- 本ペプチド製剤の皮下投与は、VIPR2の過剰な活性化によって引き起こされた動物モデルの認知機能の低下を正常レベルまで回復可能
- 本ペプチド製剤は、既存薬とは全く異なるメカニズムをもつため、統合失調症の新しい治療法の開発につながることが期待
| 北陸先端科学技術大学院大学(学長・寺野稔、石川県能美市)物質化学フロンティア研究領域の都英次郎准教授、広島大学(学長・越智光夫、広島県広島市)大学院医系科学研究科の吾郷由希夫教授、大阪大学(総長・西尾章治郎、大阪府吹田市)大学院薬学研究科の中川晋作教授、筑波大学(学長・永田恭介、茨城県つくば市)医学医療系の広川貴次教授、一丸ファルコス株式会社(社長・安藤芳彦、岐阜県本巣市)の坂元孝太郎開発2課長らの研究グループは、統合失調症の認知機能障害を回復する新薬になり得る脳移行性の皮下投与型ペプチドナノ製剤の開発に成功した(図1)。 |
 図1. 本研究の概念図
図1. 本研究の概念図
統合失調症は、幻覚や妄想などの陽性症状、意欲の低下などの陰性症状、そして注意・集中力の低下や記憶力・判断力の低下といった認知機能障害などを特徴とする精神疾患で、人口の約1%に発症し、その罹患者は日本では約80万人、全世界では2000万人以上いると言われている。既存薬は、神経伝達物質の調節に関わるメカニズムを有するもののみであり、その治療効果は限定的であり、特に認知機能障害に対する効果が乏しい。近年、神経ペプチド受容体VIPR2の過剰な活性化が統合失調症の発症に関与することが臨床研究および非臨床研究で明らかとなり、新たなメカニズムの統合失調症治療薬につながることが期待されている。本研究グループは、これまでにVIPR2を選択的に阻害するペプチドKS-133を見出していたものの(FrontPharmacol 2021,12:751587)、脳への移行性が低いことが課題であった。
本研究では、KS-133を脳に送り届けるためのナノ製剤化を検討した。血液脳関門に発現するLDL受容体関連タンパク質のLRP1は、物質を血中から脳組織に移行させる働きがある。本研究グループは、これまでにLRP1に結合するペプチドKS-487を見出していた(Biochem Biophys Rep 2022,32:101367)。そこで、1.LRP1とKS-487の複合体の構造解析を分子動力学シミュレーションで実施、2.その構造を元にKS-487を表面に提示するナノ粒子をデザイン、3.バイオイメージング試験で皮下投与されたKS-487提示ナノ粒子が脳に移行することを確認、4.KS-487提示ナノ粒子にKS-133を内包させたペプチド製剤を調製し、その効果を動物モデルで確認した。これらの結果、KS-133とKS-487を同時に搭載するナノ粒子が、KS-133を脳に効果的に移行させ、動物モデルの認知機能障害を健常レベルまで回復させることが分かった(図2)。

図2. 統合失調症モデルマウスでの認知機能を評価する試験。マウスは新しい環境や物体を積極的に探索する習性をもつ。マウスに二つの新しい物体AとBを探索させて、記憶させる。24時間後に既知物体であるBを新しい物体Cに置き換えて、マウスが物体Cをどれだけ探索するかを計測することで、マウスの物体認知、学習・記憶能力を解析する。物体AとCの総探索時間のうち、どれだけ物体Cを探索していたかを調べる識別指数を用いて評価する。数値が高いほど認知機能が高いことを意味する。統合失調症モデルマウスの識別指数は、VIPR2選択的阻害ペプチドKS-133を内包し、中枢移行性ペプチドKS-487を提示するナノ粒子の投与によって、正常マウスと同等レベルに回復する。
本研究成果は、アメリカ化学会発行の生物・化学系のトップジャーナル「JACS Au」(アメリカ化学会発行)のオンライン版に2024年6月20日に掲載された。なお、本研究は、文部科学省科研費 基盤研究(A)(23H00551)、基盤研究(B)(20H03392)、挑戦的研究(開拓)(22K18440)、国立研究開発法人科学技術振興機構(JST)研究成果最適展開支援プログラム(A-STEP)(JPMJTR22U1)、AMED橋渡し研究プログラム(JP22ym0126809)、創薬等先端技術支援基盤プラットフォーム(BINDS)(JP18am0101114、JP23ama121052、JP23ama121054)、公益財団法人発酵研究所、公益財団法人上原記念生命科学財団、ならびに北陸先端科学技術大学院大学超越バイオメディカルDX研究拠点、生体機能・感覚研究センター、広島大学トランスレーショナルリサーチセンターの支援などのもと行われたものである。
【今後の展開】
本ペプチド製剤は、VIPR2阻害という既存薬とは全く異なるメカニズムを有しており、アンメットメディカルニーズである統合失調症の認知機能障害を対象とした新薬になることが期待される。今後、細胞や動物モデルなどを用いた更なる検討、そしてヒトでの臨床試験によって、本ペプチド製剤の有効性と安全性を確認し、統合失調症の新しい治療薬として開発を進めていく。
【論文情報】
| 掲載誌 | JACS Au (アメリカ化学会誌) |
| 論文題目 | Cyclic Peptide KS-133 and KS-487 Multifunctionalized Nanoparticles Enable Efficient Brain Targeting for Treating Schizophrenia |
| 著者 | Kotaro Sakamoto*, Seigo Iwata, Zihao Jin, Lu Chen, Tatsunori Miyaoka, Mei Yamada, Kaiga Katahira, Rei Yokoyama, Ami Ono, Satoshi Asano, Kotaro Tanimoto, Rika Ishimura, Shinsaku Nakagawa, Takatsugu Hirokawa, Yukio Ago*, and Eijiro Miyako* |
| 掲載日 | 2024年6月20日 |
| DOI | https://doi.org/10.1021/jacsau.4c00311 |
令和6年6月27日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2024/06/27-1.html革新的ポリマーを用いたタンパク質凝集阻害メカニズムの解明 ―タンパク質医薬品製造の効率化や神経変性疾患治療への応用に期待―

  |
国立大学法人 国立大学法人東京工業大学 |
革新的ポリマーを用いたタンパク質凝集阻害メカニズムの解明
―タンパク質医薬品製造の効率化や神経変性疾患治療への応用に期待―
ポイント
- 双性イオンポリマー(PSPB)によるタンパク質凝集阻害の複雑な分子メカニズムを先駆的に解明した。
- PSPBは、多様なタンパク質の熱凝集に対して高い保護活性を持ち、PSPBとタンパク質の相互作用を実験及びシミュレーションにより包括的かつ詳細に検討した結果、弱く可逆的な結合の重要性を明らかにした。また、PSPBはタンパク質と弱く可逆的に相互作用することで、凝集経路を妨げ、凝集性中間体の形成を阻止することも明らかとなった。
- タンパク質治療薬の安定化と長期保存を実現する可能性を見出した。
- 将来的にはアルツハイマーなどの神経変性疾患の治療への応用も期待される。
| 北陸先端科学技術大学院大学(学長・寺野稔、石川県能美市)物質化学フロンティア研究領域の松村和明教授、ラジャンロビン元助教及びZHAO, Dandan研究員(超越バイオメディカルDX研究拠点)は、東京工業大学(学長・益一哉、東京都目黒区)生命理工学院生命理工学系の古田忠臣助教と共同で、双性イオンポリマーによるタンパク質凝集阻害メカニズムの解明に成功した。 本研究グループが合成したスルホベタインポリマーと呼ばれる双性イオン高分子は、タンパク質と弱く可逆的に相互作用し、凝集経路を妨げることで凝集性中間体の形成を阻止し、有害な凝集を防ぐ。この画期的な発見は、タンパク質治療薬を進歩させ、タンパク質のミスフォールディングに関連する様々な症状に対する新規治療法を開発する上で、計り知れない可能性を秘めている。 本成果は、2024年5月30日11時(米国東部標準時間)にCell Press発行「Cell Reports Physical Science」オンライン版に掲載された。 |
【研究の背景】
タンパク質の凝集は、アルツハイマー病、パーキンソン病、ハンチントン病などの神経変性疾患の主な原因とされている。また、タンパク質医薬品の生産と保管中に凝集が発生すると、薬剤の活性と有効性が失われる可能性がある。従来の方法では、これらの凝集を防ぐことは困難であり、効果的な安定化手法の開発が求められていた。
【研究内容】
本研究グループは、双性イオン高分子注1の一種であるスルホベタインポリマー(PSPB)及びその疎水性誘導体がタンパク質凝集を抑制するメカニズムを解明した。(図1)。PSPBはタンパク質と弱く相互作用し、凝集経路を妨げることで凝集性中間体の形成を阻止する。実験により、PSPBがインスリンやリゾチームなどの複数のタンパク質を熱ストレスから効果的に保護することが示された。特に、疎水性残基を導入したPSPBは、タンパク質の凝集抑制効果が著しく向上することが確認された。この効果は分子シールディング効果注2と呼ばれ、保護対象のタンパク質と保護高分子が可逆的な相互作用を示すことにより、物理的に凝集を妨げている様子が分子動力学シミュレーション注3の結果からも確認された。
【主な結果】
- PSPBの合成と特性評価:異なる疎水性モノマー(BuMA、HxMA、OcMA)を組み込んだ種々のスルホベタインポリマー(PSPB)を合成し、その特性を評価した。
- タンパク質の保護効果:インスリン、リゾチーム、乳酸脱水素酵素(LDH)をモデルタンパク質として使用し、PSPBがこれらタンパク質の凝集繊維形成を著しく抑制することを確認。分子量と疎水性が高いPSPBは、特に効果的であることが示された(図2)。
- 分子動力学シミュレーション:PSPBが分子シールドとして機能し、タンパク質分子間の距離を保ち、凝集を防ぐ効果を持つことが確認された(図3)。
- メカニズムの解明:熱分析、分光学的手法などを駆使し、PSPBによる凝集抑制効果の解明に成功した。モデルタンパク質のインスリンを加熱すると、タンパク質の高次構造がほどけるアンフォールディングが起こる。その後、さらに加熱することで凝集性の前駆体が形成され、不可逆な凝集体となる。ここにPSPBが存在することで、アンフォールディングする温度が高温側にシフトし、凝集前駆体の形成が阻害される。冷却時にはPSPBは脱離し、元の高次構造が維持される(図4)。PSPBへの疎水基の導入は、タンパク質の疎水性残基との相互作用を高める効果があり、より凝集前駆体の形成阻害効果を高めていることが示唆される。
【今後の展望】
PSPBによるタンパク質凝集抑制効果の分子メカニズムに迫った研究は初めてであり、このメカニズムにより、PSPBがタンパク質治療薬の安定化と長期保存に貢献できる可能性が示された。
さらに、この研究は新しい診断及び治療法の開発にも応用される可能性があり、将来的には幅広い疾患に対する効果的な治療法の提供が期待される。本研究グループは、今後さらにアミロイドβタンパクの凝集抑制などの研究を進め、アルツハイマー病やパーキンソン病などのタンパク質凝集が原因とされる神経変性疾患の治療や原因解明など、実用化に向けた具体的な応用方法の開発に取り組んでいく予定である。

図1 各種合成した双性イオンポリマー
スルホベタインポリマー(PSPB)にブチルメタクリレート(BuMA)、ヘキシルメタクリレート(HxMA)、オクチルメタクリレート(OcMA)を共重合したポリマーの構造を示す。

図2 インスリン溶液の凝集抑制の様子。i)加熱前、ii)加熱後、iii)PSPB添加後に加熱。
加熱することで凝集により白濁していることが確認される。一方、PSPBを添加することで白濁は抑えられる。

図3 P(SPB-r-BuMA)のモデルとしたスルホベタイン2量体にブチルメタクリレートを結合した化合物(SPB2_BuMA)とインスリンのMDシミュレーションによるスナップショット。インスリン二分子の間にモデル化合物が分子シールドとして可逆的にサンドイッチされ、凝集を妨げている様子が見られた。

図4 凝集抑制メカニズムの模式図。インスリン二量体(天然構造)が加熱により単量体に変性し、さらにアンフォールディングして立体構造が解消される。その際にポリマーがあると、分子シールディング効果により、凝集前駆体の形成を抑制し、繊維状凝集前駆体(prefibrillar aggregates)から繊維凝集体(mature fibrils)の形成を阻害する。
なお、本研究は、科研費基盤研究(B)20H04532、若手研究20K20197、23K17211、学術変革領域研究(A)21H05516、国立研究開発法人科学技術振興機構(JST)研究成果最適展開支援プログラム(A-STEP)JPMJTR20UN、文部科学省ナノテクノロジープラットフォーム事業JPMXP09S21MS1051、JPMXP09S21MS1051b、文部科学省マテリアル先端リサーチインフラ事業JPMXP1222MS1007、ならびに北陸先端科学技術大学院大学超越バイオメディカルDX研究拠点、生体機能・感覚研究センターの支援のもと行われた。
【論文情報】
| 雑誌名 | Cell Reports Physical Science |
| 題目 | Molecular mechanism of protein aggregation inhibition with sulfobetaine polymers and their hydrophobic derivatives |
| 著者 | Robin Rajan, Tadaomi Furuta, Dandan Zhao, Kazuaki Matsumura |
| 掲載日 | 2024年5月30日11時(米国東部標準時間) |
| DOI | 10.1016/j.xcrp.2024.102012 |
【用語説明】
同一分子内に正電荷と負電荷を持つ全体としては中性の高分子で、高い水和性と低い非特異的タンパク質吸着性を持つ。これにより、生体適合性が高く、医療分野やバイオテクノロジー分野で広く研究、応用されている。
Tunaccliffeらの報告によると、ある種の天然変性タンパク質が乾燥時に他のタンパク質の周りに保護相を形成し、物理的に凝集を抑制する効果のことを分子シールディング(molecular shielding)効果として説明している。
Chakrabortee S, et al., Mol. Biosys. 2012, 8, 210-219
分子系の運動を時間的に解析する手法。具体的には、原子や分子の初期位置と速度を設定し、相互作用ポテンシャルを用いてニュートンの運動方程式を解くことで、分子系の時間発展を追跡し、構造変化、相転移、拡散などの現象を解析する。例えば、タンパク質のフォールディング過程や薬物分子の結合動態、材料の熱物性などを詳細に調べることができ、生物学、化学、材料科学に広く応用されている。
令和6年5月31日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2024/05/31-1.htmleMEDX(イーメディックス)見学会のご案内 ~超越バイオメディカルDX研究拠点の力で生まれる未来~
下記のとおり、超越バイオメディカルDX研究拠点(eMEDX/イーメディックス)の見学会を開催しますので、ご案内します。
経済産業省令和3年度「産学連携推進事業費補助金(地域の中核大学の産学融合拠点の整備)」(Jイノベプラットフォーム型)の補助事業の採択を受け今年度より開設された当研究拠点は、DX・スタートアップ人材の育成、バイオメディカルベンチャーの創出を含む地域社会の発展に積極的に貢献し、他地域からの企業誘致などを通じて、能美市旭台に位置するいしかわサイエンスパークの活性化にもつながる取り組みです。データ駆動型の最先端DXを基盤として、疾病の超早期診断、創薬ツール、再生医療用バイオマテリアル、機能性食品、アンチエイジングなど多彩な業種・業界と協働して研究開発を行うための設備や体制を構築します。
当見学会では、施設紹介や研究所見学、担当教員による研究紹介などを通じて、当研究拠点について周知することを目的としています。本学のバイオメディカル研究の最先端を紹介する貴重な機会となりますので、ぜひご参加ください。
| 日 時 | 令和5年8月30日(水) 10:00~12:00 |
| 場 所 | 北陸先端科学技術大学院大学 超越バイオメディカルDX研究拠点(eMEDX/イーメディックス) 2Fシェアードオープンイノベーションルーム (石川県能美市旭台2-13/いしかわクリエイトラボ向かい) |
| 定 員 | 約20名 事前申込制 |
| プログラム | 第1部 施設紹介および見学会(撮影可) 第2部 研究紹介および拠点活用事例紹介 詳細は、別紙開催概要をご覧ください。 |
| 申込方法 | メールの件名と本文に「eMEDX見学会参加希望」と明記し、 ・所属 ・参加者氏名 ・メールアドレス(連絡先) ・後日個別相談会 希望する or 希望しない ・個別相談を希望する場合は、本学教員またはURAの氏名 上記をご記入のうえ、下記申込み先にお送りください。 |
| 申込締切 | 令和5年8月25日(金) |
| 申込み・ 問合せ先 |
北陸先端科学技術大学院大学 未来創造イノベーション推進本部 担当:山廣、竹田 E-mail:emedx@ml.jaist.ac.jp |

建物外観

最先端の研究を実現するオープンラボ

ワークスペースも完備

交流のためのシェアード
イノベーションルーム
令和5年8月10日
出典:JAIST イベント情報https://www.jaist.ac.jp/whatsnew/event/2023/08/10-1.htmlMeet up Chubu イベント「超越バイオメディカルDX研究拠点」見学会を開催
7月27日(木)、中部経済産業局および中部経済連合会主催の、連携パートナーを探索するためのオープンイノベーションプラットフォームである『Meet up Chubu』が、本学の「超越バイオメディカルDX研究拠点(eMEDX)」にて開催されました。現地参加とオンラインのハイブリッド形式で行われ、当日は約60名の多種多様な業種・業界の方々にご参加いただきました。
最初にeMEDX拠点長である物質化学フロンティア研究領域の松村 和明教授から施設概要の紹介があり、その後、eMEDX施設内のオンラインツアーをライブ配信で行いました。
続いて、松村教授、同じく物質化学フロンティア研究領域の都 英次郎准教授の研究紹介が行われました。各セッションの最後には参加者からたくさんの質問があり、活発な意見交換がなされました。
最後に、寺野稔学長からの挨拶では、eMEDXの展望について発言がありました。
eMEDXでは、本学が誇る世界トップレベルのバイオメディカル分野の研究に、スーパーコンピューターを活用したデータ駆動型のDXを組み合わせ、医療・ヘルスケア・メディカルなどに関わる広い分野でのイノベーションを目指すとともに、技術や知識をシェアして共創する「シェアードオープンイノベーション」という新しい考え方に基づき、多種多様な業種・業界の会員企業間のざっくばらんな交流を推進することで、北陸から世界のバイオメディカルを変えるイノベーションを共創していきます。

学長挨拶

松村和明 拠点長・教授

都英次郎 准教授

研究紹介の様子
| 施設に関するお問い合わせ先 北陸先端科学技術大学院大学 未来創造イノベーション推進本部 担当:山廣、竹田 〒923-1292 石川県能美市旭台1-1 E-mail:emedx@ml.jaist.ac.jp |
令和5年8月10日
出典:JAIST お知らせ https://www.jaist.ac.jp/whatsnew/info/2023/08/10-1.html大学見本市2023~イノベーション・ジャパンに本学が出展
8月24日(木)・25日(金)の2日間、東京ビッグサイト南展示棟(東京都江東区有明)で国内最大規模の産学マッチングイベントである「大学見本市2023~イノベーション・ジャパン」が開催されます。
本学からは以下の2件が出展します。
ご来場の際にはぜひお立ち寄りください。
| 日 時 | 8月24日(木) 10時00分~17時30分 8月25日(金) 10時00分~17時00分 |
| 会 場 | 東京ビッグサイト 南展示棟 南1ホール(東京都江東区有明3丁目11番1) |
| 大学等 シーズ展示 |
超越バイオメディカルDX研究拠点 物質化学フロンティア研究領域 松村和明 教授 【小間番号】H-56 高田健司 助教 【小間番号】C-68 |
詳細はこちらをご覧ください。
・イノベーション・ジャパン2023公式サイト
・イノベーション・ジャパン2023出展課題一覧
eMEDX(イーメディックス)見学会 ~超越バイオメディカルDX研究拠点の力で生まれる未来~
下記のとおり、超越バイオメディカルDX研究拠点(eMEDX/イーメディックス)の見学会を開催しますので、ご案内します。
経済産業省令和3年度「産学連携推進事業費補助金(地域の中核大学の産学融合拠点の整備)」(Jイノベプラットフォーム型)の補助事業の採択を受け今年度より開設された当研究拠点は、DX・スタートアップ人材の育成、バイオメディカルベンチャーの創出を含む地域社会の発展に積極的に貢献し、他地域からの企業誘致などを通じて、能美市旭台に位置するいしかわサイエンスパークの活性化にもつながる取り組みです。データ駆動型の最先端DXを基盤として、疾病の超早期診断、創薬ツール、再生医療用バイオマテリアル、機能性食品、アンチエイジングなど多彩な業種・業界と協働して研究開発を行うための設備や体制を構築します。
当見学会では、施設紹介や研究所見学、担当教員による研究紹介などを通じて、当研究拠点について周知することを目的としています。本学のバイオメディカル研究の最先端を紹介する貴重な機会となりますので、ぜひご参加ください。
| 日 時 | 令和5年6月19日(月) 15:00~17:00 |
| 場 所 | 北陸先端科学技術大学院大学 超越バイオメディカルDX研究拠点(eMEDX/イーメディックス) 2Fシェアードオープンイノベーションルーム (石川県能美市旭台2-13/いしかわクリエイトラボ向かい) |
| 定 員 | 約30名 事前申込制 |
| プログラム | 第1部 施設紹介および見学会(撮影可) 第2部 研究紹介および拠点活用事例紹介 第3部 個別面談 詳細は、別紙開催概要をご覧ください。 |
| 申込方法 | メールの件名と本文に「eMEDX見学会参加希望」と明記し、 ・所属 ・参加者氏名 ・メールアドレス(連絡先) ・個別相談会 希望する or 希望しない ・個別相談を希望する場合は、本学教員またはURAの氏名 上記をご記入のうえ、下記申込み先にお送りください。 |
| 申込締切 | 令和5年6月12日(月) |
| 申込み・ 問合せ先 |
北陸先端科学技術大学院大学 未来創造イノベーション推進本部 担当:山廣、竹田 E-mail:emedx@ml.jaist.ac.jp |

建物外観

最先端の研究を実現するオープンラボ

ワークスペースも完備

交流のためのシェアード
イノベーションルーム
令和5年6月8日
出典:JAIST イベント情報https://www.jaist.ac.jp/whatsnew/event/2023/06/08-1.html固体電解質薄膜トランジスタを用いたバイオセンサの製品化に着手 ~短時間で複数の核酸・病原体を同時に検出~

  |
| 三菱マテリアル株式会社 国立大学法人北陸先端科学技術大学院大学 |
固体電解質薄膜トランジスタを用いたバイオセンサの製品化に着手
~短時間で複数の核酸・病原体を同時に検出~
三菱マテリアル株式会社と北陸先端科学技術大学院大学(石川県能美市) バイオ機能医工学研究領域の高村禅教授、廣瀬大亮助教は、共同で新規の固体電解質薄膜トランジスタを用いたバイオセンサを開発し、実用化に向けた製品開発に着手しました。
医療の分野における遺伝子検査では、一般的にPCR(Polymerase Chain Reaction)法など核酸を増幅して検査する方法が用いられていますが、検査機器が高価であり、また、大型のため用途が限定されています。
三菱マテリアルでは、従来より金属や酸化物など様々な材料に薄膜を形成するための研究開発を行っており、湿式成膜による薄膜材料開発に関する高い技術力を有しています。このたびの共同開発ではその技術を応用し、検知部に独自に開発した固体電解質薄膜トランジスタを用いた新たなバイオセンサを開発しました(模式図参照)。
本バイオセンサでは、微小な電荷による電圧変化を検出することでPCRなどの増幅法に比べて短時間で検査結果を得ることができます。また、微細加工技術を利用してセンサ素子を並列に複数個配列することができるため、複数の核酸・病原体の同時検出が可能となります。さらに、固体電解質薄膜トランジスタ自体が小さいため、バイオセンサの小型化が可能であり今後も用途の拡大が見込めます。
今後は測定可能な核酸の種類を拡張するとともに、複数の種類を含む病原体を同時に検出可能なセンサの製品化に取り組み、実用化に向けた製品開発を推進します。
三菱マテリアルグループは、「人と社会と地球のために」という企業理念のもと、これからも非鉄金属素材およびライフヘルスケア分野に付加価値の高い製品の開発・提供を通じて、豊かな社会の構築に貢献してまいります。

新開発のバイオセンサ
【性能】
固体電解質薄膜トランジスタの表面に負の電荷を有する核酸が特異的に吸着した場合、表面電荷の変化が生じ、変化に対応した電圧変化を大きなシグナルとして読み取ることが可能です。(図1参照)

図1 新規開発品によるシグナル増強について
固体電解質薄膜トランジスタを用いて、大腸菌に含まれる稀薄な核酸について、増幅することなく検出できることを確認しました。(図2参照)。

図2 大腸菌検出結果
【関連情報】
本リリースで紹介している固体電解質薄膜トランジスタは、以下のJournalに掲載されています。
Journal of Applied Physics 127, 064504 (2020)
令和5年5月19日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2023/05/19-1.htmlマイクロロボットを"流れ"作業で迅速に作製 -生体分子モーターによる人工筋肉で自在にプリント・動的再構成可能に-

  |
国立大学法人 大阪大学 国立大学法人 北陸先端科学技術大学院大学 国立大学法人東海国立大学機構 岐阜大学 |
マイクロロボットを"流れ"作業で迅速に作製
-生体分子モーターによる人工筋肉で自在にプリント・動的再構成可能に-
【ポイント】
- マイクロ流路※1の中で、光に応答する材料を流しながら、マイクロロボット※2のボディと駆動源となるアクチュエータ※3を連続的に生産・組み立てを行う「マイクロロボットその場組み立て法」を開発
- 様々な機能をもつマイクロロボットの迅速な作製に成功
- より高機能なマイクロロボットの実現と、マイクロロボットの量産化に期待
【概要】
| 大阪大学・大学院工学研究科の森島圭祐教授、王穎哲特任研究員(常勤)は、 北陸先端科学技術大学院大学・先端科学技術研究科 バイオ機能医工学研究領域の平塚祐一准教授、岐阜大学・工学部の新田高洋教授との共同研究で、マイクロ流路内で、マイクロロボットの部品をプリント成形し、その場で組み立てることに成功しました。マイクロロボットの機械構造は光応答性ハイドロゲル※4でつくられ、アクチュエータは同じチームが開発した生体分子モーターからなる人工筋肉を利用しました。このアクチュエータと機械部品をマイクロ流路内で組み立てることにより、マイクロロボット製造の柔軟性と効率が向上しました。この方法で、様々な機能のマイクロロボットが実現されました。また、この成果により、これまで困難であった、特に柔軟な構造を持つマイクロソフトロボットの実現や、マイクロロボットの量産化が期待されます。 本研究成果は、2022年8月24日午後2時(米国時間)に発行される科学雑誌「Science Robotics」の表紙を飾りました。 |
【研究の背景】
マイクロロボット、特に柔軟な構造を持つロボットは、生物医学などの分野で非常に幅広い応用の可能性があるものの、小さなロボットにアクチュエータなど様々な機械部品を組み込むことは困難で、高機能のマイクロロボット開発の障害となっています。従来の方法では、通常、機械構造やアクチュエータなど、マイクロロボットの様々な部品を異なる場所で製造し、一つ一つ組み上げていくピック アンド プレース アセンブリによってマイクロロボットがつくられていました。この方法は時間と労力がかかり、また多くの制限があることが課題となっています。
【研究の内容】
本研究では、自然界の生体内システムの自己組織化プロセスに着想を得て、2021年に発表したプリント可能な生体分子モーターからなる人工筋肉(1)(2)に基づき、ロボット部品をその場で加工・組み立てしてマイクロロボットを製造する方法を開発しました。マイクロ流路内で、マスクレスリソグラフィー※5により、ハイドロゲル材料の機械的構造をプリントし、次に生体分子モーターからなる人工筋肉がハイドロゲル機構の狙った位置に直接プリントすることで、機構を駆動して目的の仕事を実施します(図1) 。 このその場組み立てにより、マイクロロボットを迅速に次々と生産することができます。
また、マイクロロボットに新しい人工筋肉を再プリントすることにより、アクチュエータを迅速に動的再構成し、複雑な仕事を行うマイクロロボットを実現しました(図2)。
さらに、生体分子モーターを使用する本研究とは異なる、生きた筋肉細胞を用いるアプローチとして細胞ハイブリッドロボット※6が注目されています。細胞ハイブリッドロボットは、柔軟性が高く、環境負荷が低いという利点があるものの、筋肉細胞の培養に数日かかってしまうという問題があります。本研究では、設計の柔軟性を向上させながら、製造プロセスを大幅に簡素化することに成功しました。今後のオンチッププリンティング技術の向上や人工筋肉の性能向上により、現在の細胞ハイブリッドロボットのボトルネックを打破し、実用化に向けた一歩を踏み出すことが期待される手法であると考えています。
(1) https://www.nature.com/articles/s41563-021-00969-6
(2) https://www.jaist.ac.jp/whatsnew/press/2021/04/20-1.html

図1 マイクロロボットその場組み立て法

図2 その場組み立て法によって製造したマイクロロボットが生体分子モーターからなる人工筋肉によって駆動する様子
【本研究成果が社会に与える影響(本研究成果の意義)】
今回の研究により、自然界の生体分子モーターによって運動が創発する自己組織化現象をオンチップ微小空間上で工学的に制御し、自在にデザインできる加工プロセスをボトムアップ的な発想でより簡便に実現できました。これにより、これまで超微小部品をトップダウン的に組み立てることが大きなボトルネックであったために遅れていた、マイクロロボットの組み立てやマイクロソフト機構のオンデマンド生産が可能になりました。今後、様々な機能を付与したマイクロロボットがオンチップ上で連続的にオンデマンド生産することが可能になり、化学エネルギーだけで駆動する超小型マイクロロボットが健康医療応用など様々な分野に展開、波及していくことが期待できます。
【特記事項】
本研究は、日本学術振興会(JSPS)科研費 基盤研究(S)(課題番号22H04951)、基盤研究(A)(課題番号22H00196)、基盤研究(B)(課題番号19H02106)、学術変革領域研究(A)(課題番号21H05880)、挑戦的萌芽研究(課題番号21K18700)、新エネルギー・産業技術総合開発機構(NEDO)「次世代人工知能・ロボット中核技術開発」(JPNP15009)の支援を受けて行われました。
【論文情報】
| タイトル | In situ integrated microrobots driven by artificial muscles built from biomolecular motors |
| 著者名 | Yingzhe Wang, Takahiro Nitta, Yuichi Hiratsuka ,and Keisuke Morishima |
| DOI | https://www.science.org/doi/10.1126/scirobotics.aba8212 |
【用語説明】
ガラスや高分子材料で作製した数ミリメートルから数マイクロメートルの流路で、効率的に化学反応などを起こすことができる。微小なバイオセンサーや化学分析装置に利用されている。
数ミリメートル以下のサイズのロボットで、医療などへの応用が期待されている。
モーターやエンジンなどのように電気や化学エネルギーなどを利用して、動きや力を発生する装置。
紫外線などの光を照射することでゼリー状に固まる物質。
光照射による微細加工技術で、半導体デバイスなどの製造に利用されている。
培養細胞と機械部品を融合させて作製したロボット。
【SDGs目標】

【参考URL】
森島圭祐教授 研究者総覧URL https://rd.iai.osaka-u.ac.jp/ja/90351526dc15ef59.html
生命機械融合ウェットロボティクス領域URL http://www-live.mech.eng.osaka-u.ac.jp/
令和4年8月26日
出典:JAIST プレスリリース https://www.jaist.ac.jp/whatsnew/press/2022/08/26-1.html物質化学フロンティア研究領域の松村教授らの論文がBiomacromolecules誌の表紙に採択
物質化学フロンティア研究領域の松村研究室による論文が、米国化学会(American Chemical Society :ACS)刊行のBiomacromolecules誌の表紙(Supplementary cover)に採択されました。本研究成果は、物質・材料研究機構および産業技術総合研究所との共同研究によるものです。
■掲載誌
ACS Biomacromolecules, 2022Volume 23, Issue 8
表紙掲載日2022年8月8日
■著者
Chiaki Yoshikawa, Keita Sakakibara, Punnida Nonsuwan(松村研究室修了生), Miwako Shobo, Xida Yuan(松村研究室修了生), Kazuaki Matsumura
■論文タイトル
Cellular Flocculation Driven by Concentrated Polymer Brush-Modified Cellulose Nanofibers with Different Surface Charges
■論文概要
今回の論文は、濃厚ポリマーブラシを表面グラフトしたセルロースナノファイバーが細胞と相互作用して凝集体を形成する際の表面電荷の影響について詳細に議論したものです。その結果、アニオン性のポリマーブラシをグラフトすることで良好な細胞凝集塊の形成がみられました。
本研究結果は、再生医療用三次元細胞足場材料への応用が期待できます。
本発表は、物質・材料研究機構、産業技術総合研究所との共同研究による成果です。
表紙詳細:https://pubs.acs.org/toc/bomaf6/23/8
論文詳細:https://pubs.acs.org/doi/full/10.1021/acs.biomac.2c00294

令和4年8月9日
出典:JAIST お知らせ https://www.jaist.ac.jp/whatsnew/info/2022/08/09-1.html